首页 >
行业动态 > 锆基金属有机框架介导选择性蛋白水解的结构与机理基础
锆基金属有机框架介导选择性蛋白水解的结构与机理基础
鲁汶大学Tatjana N. Parac-Vogt、Francisco de Azambuja团队以锆基 UiO‑66 金属有机框架为研究对象,结合高分辨质谱与分子模拟,系统探究其对细胞色素 c 的选择性水解机制。研究发现 UiO‑66 优先水解甘氨酸、苏氨酸、赖氨酸邻近肽键,尤其当三者邻近时呈现协同识别效应;甘氨酸的小位阻利于肽键与 Zr₆O₈活性位点精准配位,苏氨酸、赖氨酸通过氢键与静电作用介导底物结合与取向。该选择性区别于离散锆基氧簇的天冬氨酸偏好,证实 MOF 三维骨架对水解行为的关键调控作用,为框架工程化纳米酶用于靶向蛋白剪切提供机理支撑,推动其在蛋白质组学、蛋白工程及治疗开发中的应用。
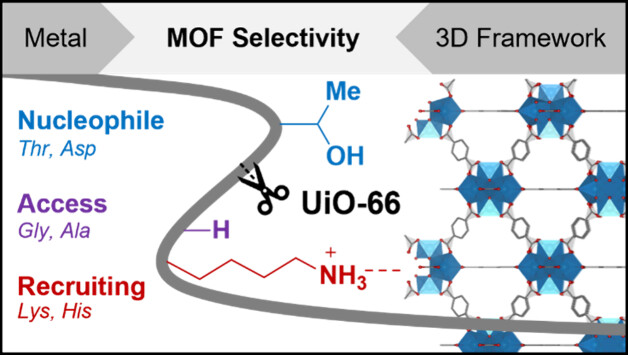
研究背景
1. 行业核心问题
天然蛋白酶(如胰蛋白酶)易自切、片段过短、序列覆盖率低;化学试剂(如溴化氰)毒性大、条件苛刻、易修饰氨基酸;现有锆基纳米酶机理不明,位点选择性不清,难以满足高通量蛋白质组学需求。
2. 现有研究方案
学者已证实锆基 MOF 具备蛋白水解活性,离散 Zr₆簇对天冬氨酸位点具特异性,可产生适合中下层蛋白质组学的片段;但 MOF 三维框架对选择性的贡献、界面相互作用本质尚未阐明,设计多依赖经验。
3. 本文创新思路
以稳定的 UiO‑66 为模型、细胞色素 c 为底物,采用质谱 + 分子对接联合手段,明确水解位点偏好与分子机制;揭示缺陷位点增强活性的规律,建立氨基酸残基作用与骨架效应的关联,为理性设计高选择性 MOF 基人工蛋白酶提供理论依据。
实验部分
1. UiO‑66 的合成与活化
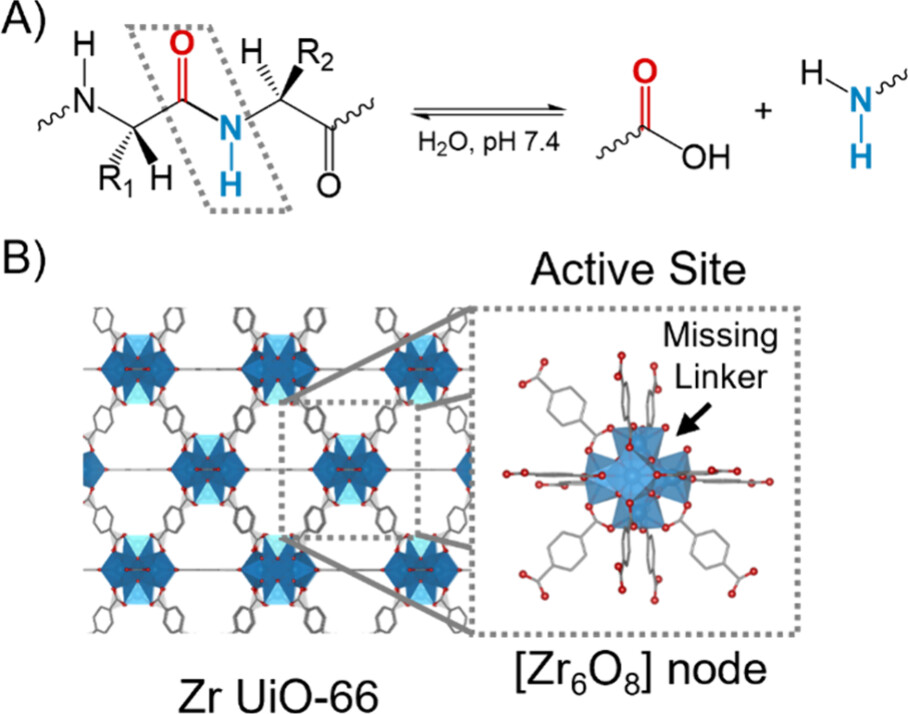
以 ZrCl₄与对苯二甲酸为原料,DMF 为溶剂,盐酸调控,80℃反应 24h;经 DMF、乙醇、甲醇洗涤,旋转蒸发干燥,150℃真空活化过夜,得到缺陷型 UiO‑66,平均粒径 229nm,每个 Zr₆节点含 1 个缺陷。
2. 蛋白水解实验
配置细胞色素 c 与肌红蛋白溶液,pH 调至 7.4,加入 UiO‑66,60℃、1200rpm 孵育 24h;设置无 MOF 对照组,排除自发降解干扰。
3. 洗脱与前处理
加入 0.5M Na₂CO₃,25℃孵育 30min,离心去除 Zr‑碳酸盐沉淀,上清调回中性,用于下游分析。
4. 分离与鉴定
采用 SDS‑PAGE 初步判断片段分子量;结合 HPLC‑MS/MS 精准定位剪切位点,统计残基偏好,验证选择性通用性。
实验突破:首次明确 UiO‑66 对 Gly/Thr/Lys 邻近位点的特异性,区别于离散 Zr 簇的 Asp 选择性,实现长肽段可控剪切,适配中下层蛋白质组学。
分析测试
1. 材料结构表征
PXRD 证实 UiO‑66 结晶度良好;N₂吸附测得 BET 比表面积优异,孔径约 1.6nm;TGA、ATR‑FT‑IR、SEM 验证组成、热稳定性与形貌;¹H NMR 确认配体结构与缺陷存在。
2. 电泳分析
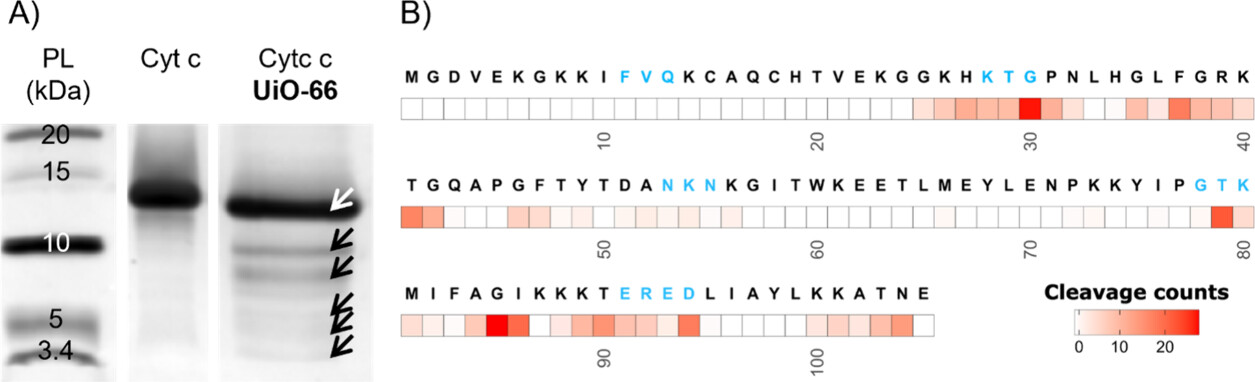
细胞色素 c 水解产生约 10.6、8.9、5.8、3.4、1.5kDa 五条特征条带,对应特定区域剪切,与质谱位点高度吻合。
3. 质谱定量分析
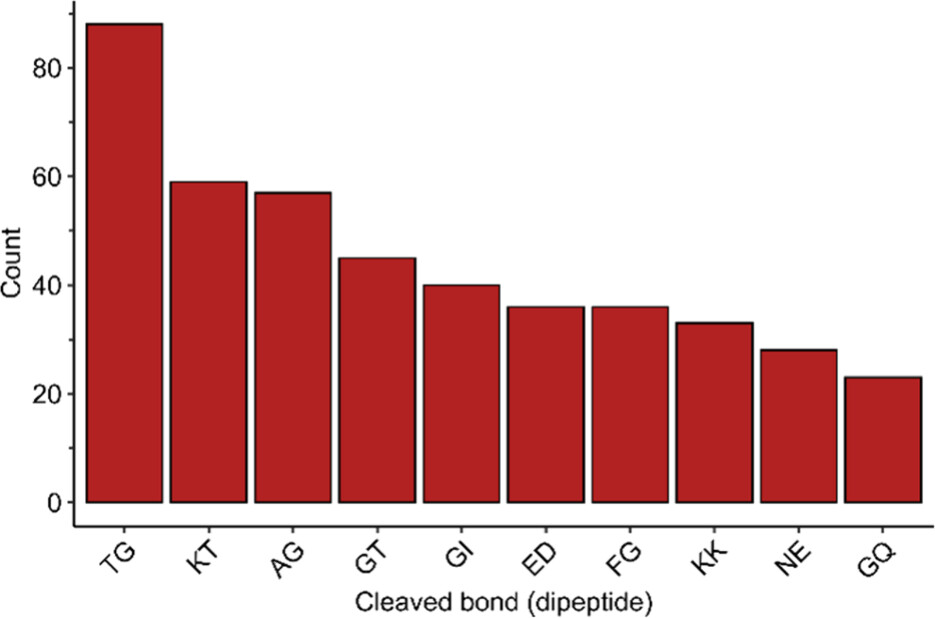
HPLC‑MS/MS 确定高频剪切位点集中于 25–42 与 79–95 区域,Thr‑Gly、Lys‑Thr、Ala‑Gly、Gly‑Thr 为 Top4 剪切键;Gly 在前十位点中占 6 个,Lys、Thr 高频出现,证实残基协同偏好。
4. 蛋白通用性验证
肌红蛋白实验显示同样偏好 Gly/Lys/His 位点,位点集中于蛋白表面,证明选择性具有普适性。
结果揭示:UiO‑66 表面负电(pI≈5.5)与 Lys/Arg 静电吸引,Gly 小位阻降低空间位阻,Thr 提供羟基辅助,三者协同实现位点选择性。
机理分析
1. 结合与识别机制
分子对接显示 UiO‑66 优先结合含 Gly/Thr/Lys 的松散环与 α‑螺旋区;缺陷位点提升结合能,Zr₆O₈簇与肽键距离缩短至 3.0–3.2Å,利于活化。
2. 残基分工机制
Lys/Arg 通过静电作用招募 MOF 靠近蛋白;Gly 无侧链,允许活性位点精准接近肽键;Thr 羟基形成氢键并提供亲核位点,降低水解能垒。
3. 骨架效应
离散 Zr₆簇倾向 Asp 位点,UiO‑66 因三维骨架、配体环境与缺陷位点,重塑选择性,证明框架结构决定位点偏好。
4. 催化路径
Zr (IV) 活化肽键羰基,配合 Thr 介导的分子内重排,实现高效水解,反应主要发生在 MOF 外表面。
总结
本工作建立质谱 + 分子模拟联用方法,阐明 UiO‑66 选择性蛋白水解的分子机理,明确 Gly/Thr/Lys 协同识别机制,揭示三维框架与缺陷对选择性的调控作用。
UiO‑66 可产生长肽片段,优于胰蛋白酶,适配中下层蛋白质组学;在细胞色素 c 与肌红蛋白上验证通用性,具备规模化应用潜力。
提出通过框架工程、缺陷调控与配体修饰理性优化选择性的策略,为 MOF 基纳米酶设计提供新范式,拓展其在生物分析、疾病诊疗等领域的应用。
文章标题:Structural and Mechanistic Basis of Selective Proteolysis by Zr-Based Metal–Organic Frameworks
文章作者:Siene SwinnenMaxim LoxBartosz TrzaskowskiTamara VasovicTanja Cirkovic VelickovicFrancisco de Azambuja*Tatjana N. Parac-Vogt*
DOI:10.1021/acs.chemmater.6c00428
文章链接:https://pubs.acs.org/doi/10.1021/acs.chemmater.6c00428
本文为科研用户原创分享,用于学术宣传交流,具体细节请查阅原文。如有错误、侵权,请联系修改删除,未经允许不得复制转载。



