首页 >
行业动态 > 【NU-1000纳米片】金属有机框架纳米片的自适应孔道形变用于强化酶催化
【NU-1000纳米片】金属有机框架纳米片的自适应孔道形变用于强化酶催化
摘要
中山大学陈国胜、欧阳锋钢,华南理工韩宇、重庆大学刘玲梅等联合报道的研究(J. Am. Chem. Soc. 2026, DOI: 10.1021/jacs.5c22730)中选用NU-1000、NU-1008两种同构锆基MOF纳米片为载体,包埋细胞色素c(Cyt c)构建双功能氧化生物催化剂,首次直观证实MOF“刚性”孔道的自适应形变行为。借助低剂量电子显微镜,直接观测到非极性NU-1000孔道扩张、极性NU-1008孔道收缩的差异化响应,孔道扩张促使Cyt c的血红素铁从六配位(S=1/2)转变为高活性五配位(S=3/2),催化氧化活性较游离酶提升一个数量级。该生物催化剂通过高价铁(IV)-氧中间体机制,实现有毒有机污染物的高效降解,性能远超现有纳米催化剂。本研究打破载体为静态惰性支架的传统认知,为孔道限域下酶催化反应的机制解析与材料设计提供全新思路。
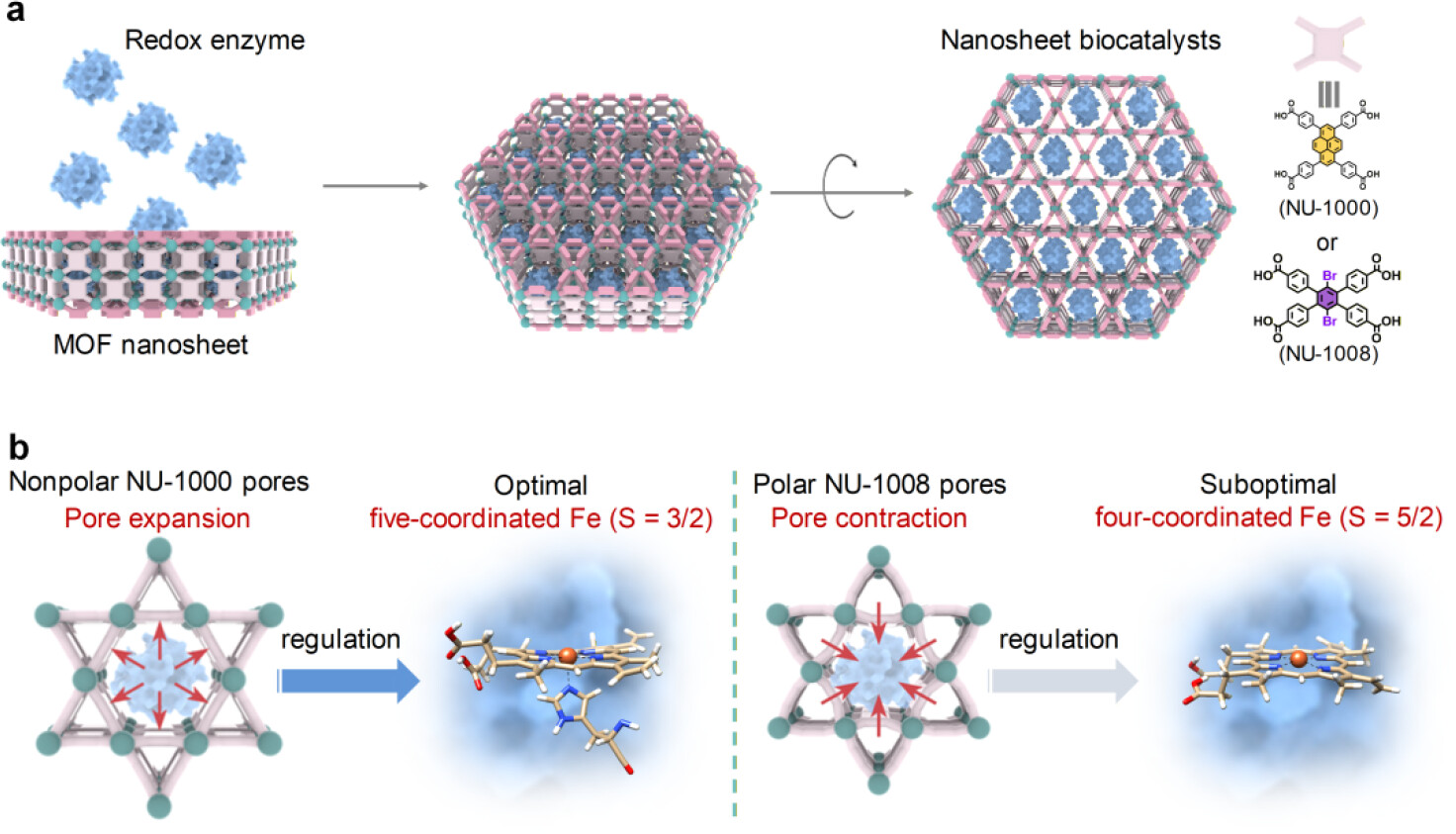
研究背景
1. 行业问题:游离酶在非生理条件下稳定性差、难以回收,限制工业化应用;MOF作为酶载体虽能提升稳定性,但学界普遍将其视为静态惰性支架,忽略主客体动态相互作用;且缺乏原子级观测手段,无法解析孔道结构与酶活性的构效关系,难以实现酶活性精准调控。
2. 现有方案:现有研究多聚焦MOF孔道尺寸、比表面的静态调控,仅实现酶活性小幅提升(最高1.25倍);针对同构MOF的界面极性调控研究匮乏,且未实现孔道动态形变的直接观测,高价铁氧中间体介导的催化机理未得到系统验证。
3. 本文创新:
1) 设计同构、极性差异化的NU-1000/NU-1008 MOF纳米片,利用化学切割法制备超薄纳米片(15 nm),便于电子显微镜表征;首次通过低剂量iDPC-STEM直接观测孔道自适应形变;
2) 揭示孔道形变调控血红素铁配位构型的机制,实现酶活性最高11.26倍提升;构建连续流膜反应器,验证实际水污染治理应用潜力。
实验部分
1. MOF纳米片可控制备:采用化学切割策略,以[1,1′,3′,1″-三联苯]-4,4″-二羧酸TPCA为切割分子,抑制晶体沿[001]方向生长,制备厚度15-70 nm可调的六方形NU-1000、NU-1008纳米片,筛选15 nm超薄纳米片用于后续实验,保证电子束穿透与孔道结构观测。
2. 酶包埋与负载量优化:在pH=7.4的Tris缓冲液、25℃条件下,将Cyt c浸渍负载于MOF纳米片孔道,12 h达负载饱和;NU-1000负载量达41.19 wt%,NU-1008仅12.51 wt%,升温至80℃后NU-1008负载量接近理论最大值37.03 wt%。
3. 酶催化活性测试:以H₂O₂为氧化剂,选用ABTS、多巴胺等四种底物,对比游离Cyt c、Cyt c@NU-1000、Cyt c@NU-1008的催化性能;Cyt c@NU-1000催化效率为游离酶的2.54-11.26倍,Cyt c@NU-1008仅小幅提升。
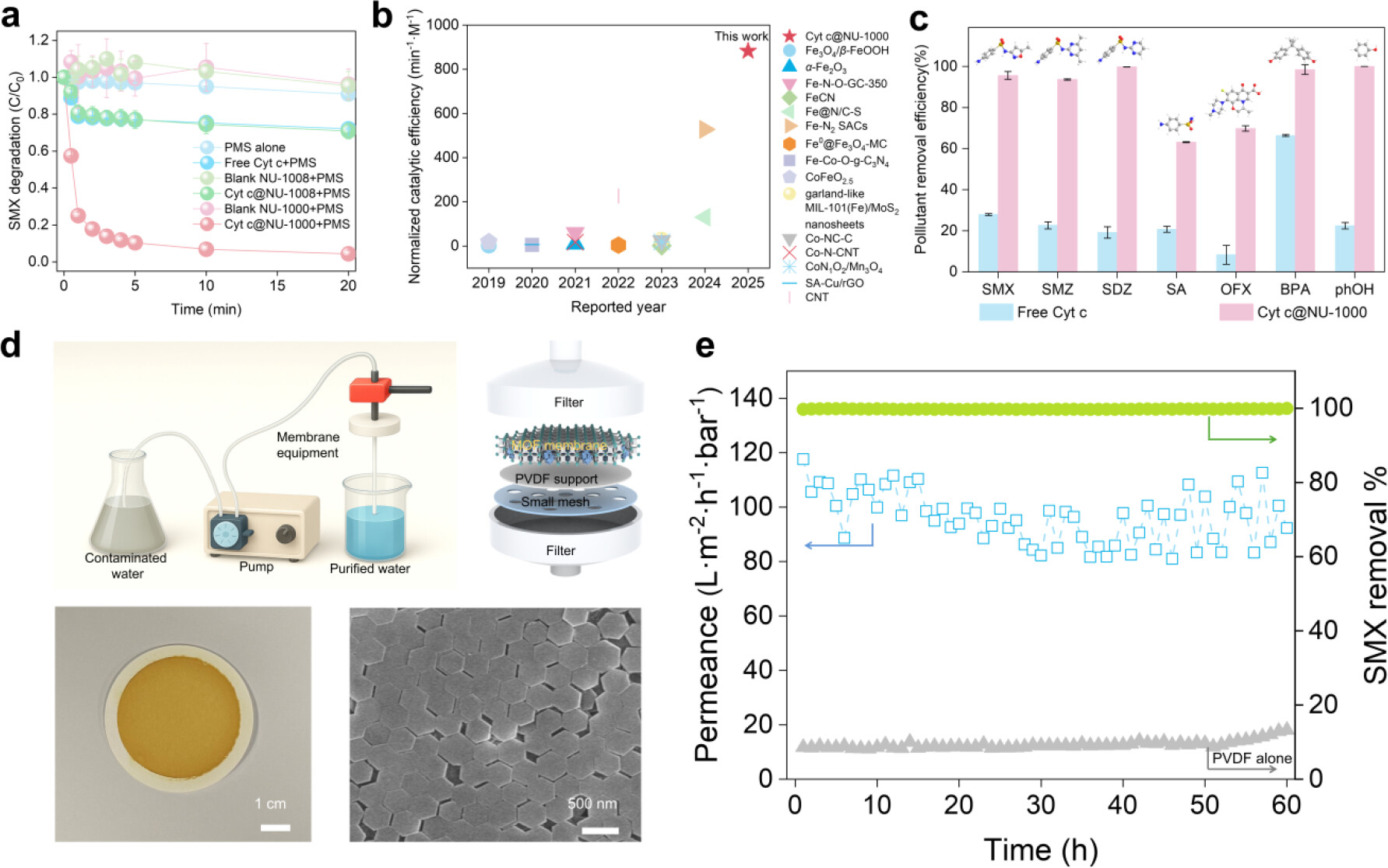
4. 有毒污染物降解:以PMS为氧化剂,磺胺甲恶唑(SMX)为模型污染物,Cyt c@NU-1000在20 min内降解率超95%,速率常数1.385 min⁻¹,远超游离酶与现有催化剂;拓展至磺胺二甲嘧啶、双酚A等多种污染物,降解效率均提升1.5-8.4倍。
5. 构建连续流膜反应器:采用挥发诱导法,将改性Cyt c@NU-1000与PAN复合,在PVDF基底上制备650 nm厚催化膜,组装连续流反应器;水通量达96.2 L m⁻² h⁻¹ bar⁻¹,60 h连续运行SMX去除率保持99%以上,无酶泄漏。
实验突破:首次实现MOF孔道自适应形变的直接可视化观测,酶活性提升幅度远超现有体系;构建的催化膜具备长效稳定性,实现实验室研究到实际应用的跨越。
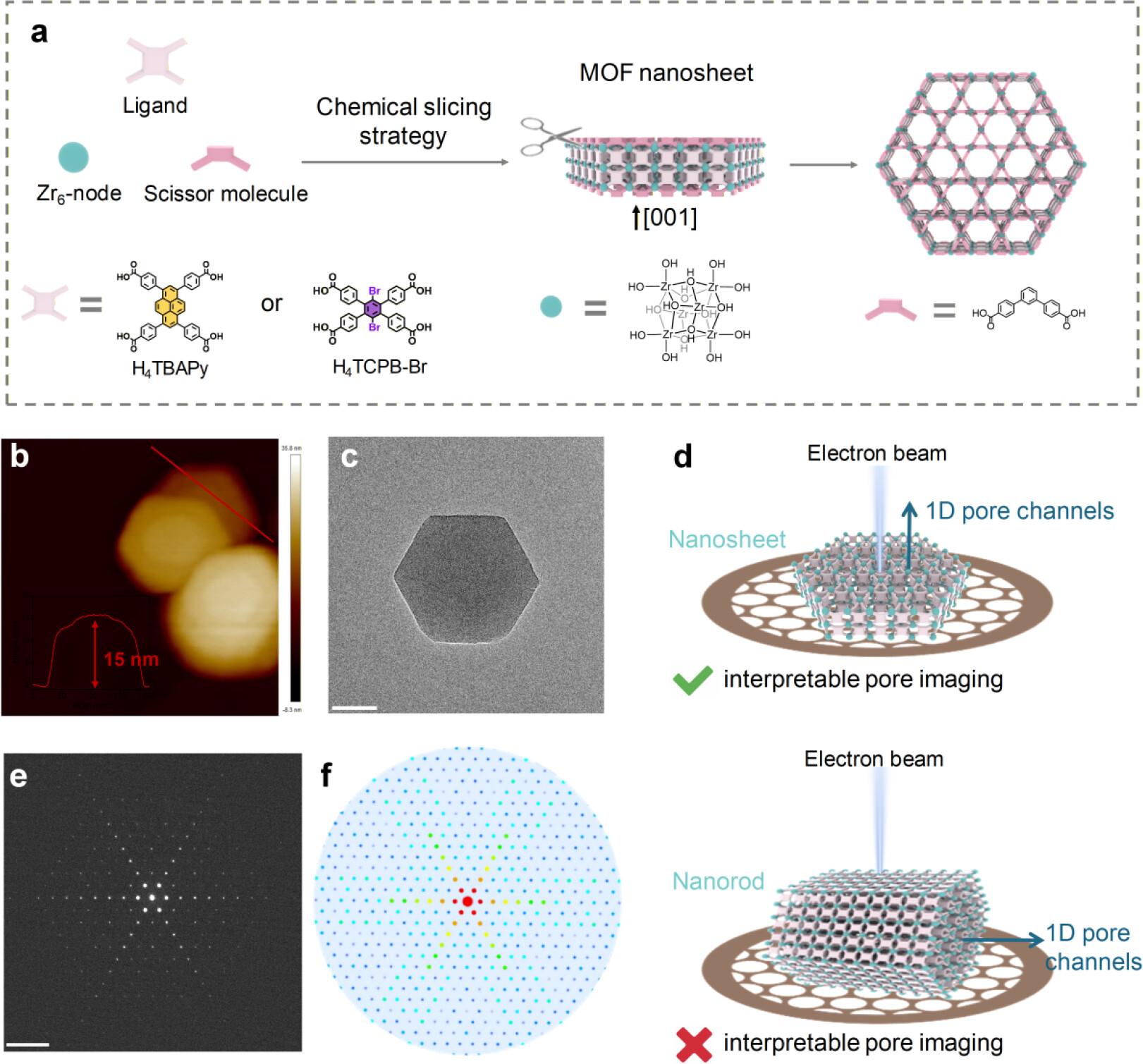
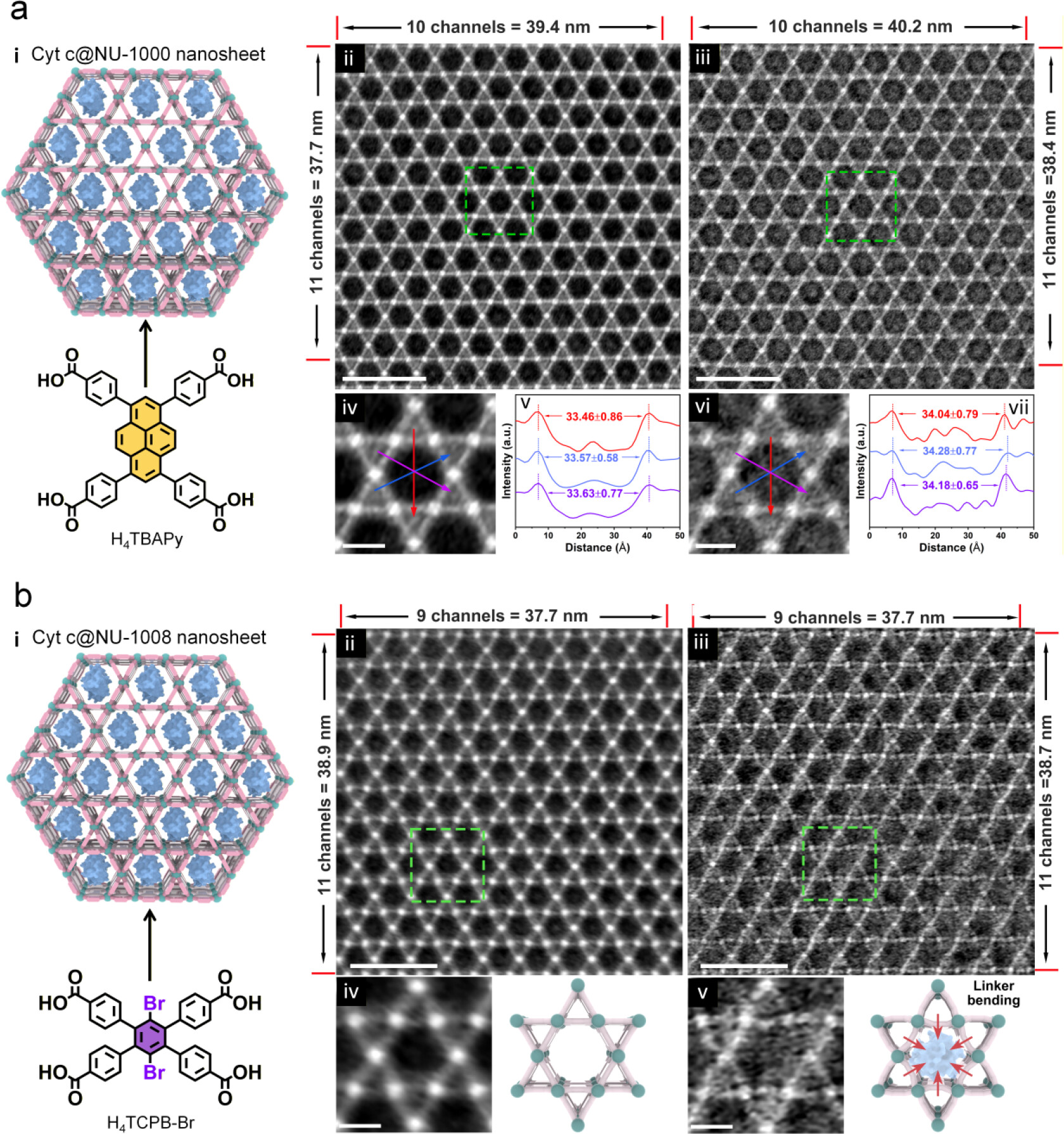
分析测试
1. 形貌与结构:AFM显示纳米片厚度15.2±0.8 nm,TEM/SAED证实高结晶性与csq拓扑;低剂量iDPC-STEM观测到Cyt c@NU-1000孔道扩张1.5%-2.0%,晶胞参数a增大2.0%;Cyt c@NU-1008配体弯曲、孔道收缩,晶胞无变化。
2. 孔隙与负载性能:77K N₂吸附测试表明,纯NU-1000比表面1985 m²/g,孔容1.55 cm³/g,孔径2.6 nm;纯NU-1008比表面1670 m²/g,孔容1.10 cm³/g;酶负载后两者孔容大幅下降,NU-1000下降更显著,与高负载量一致。
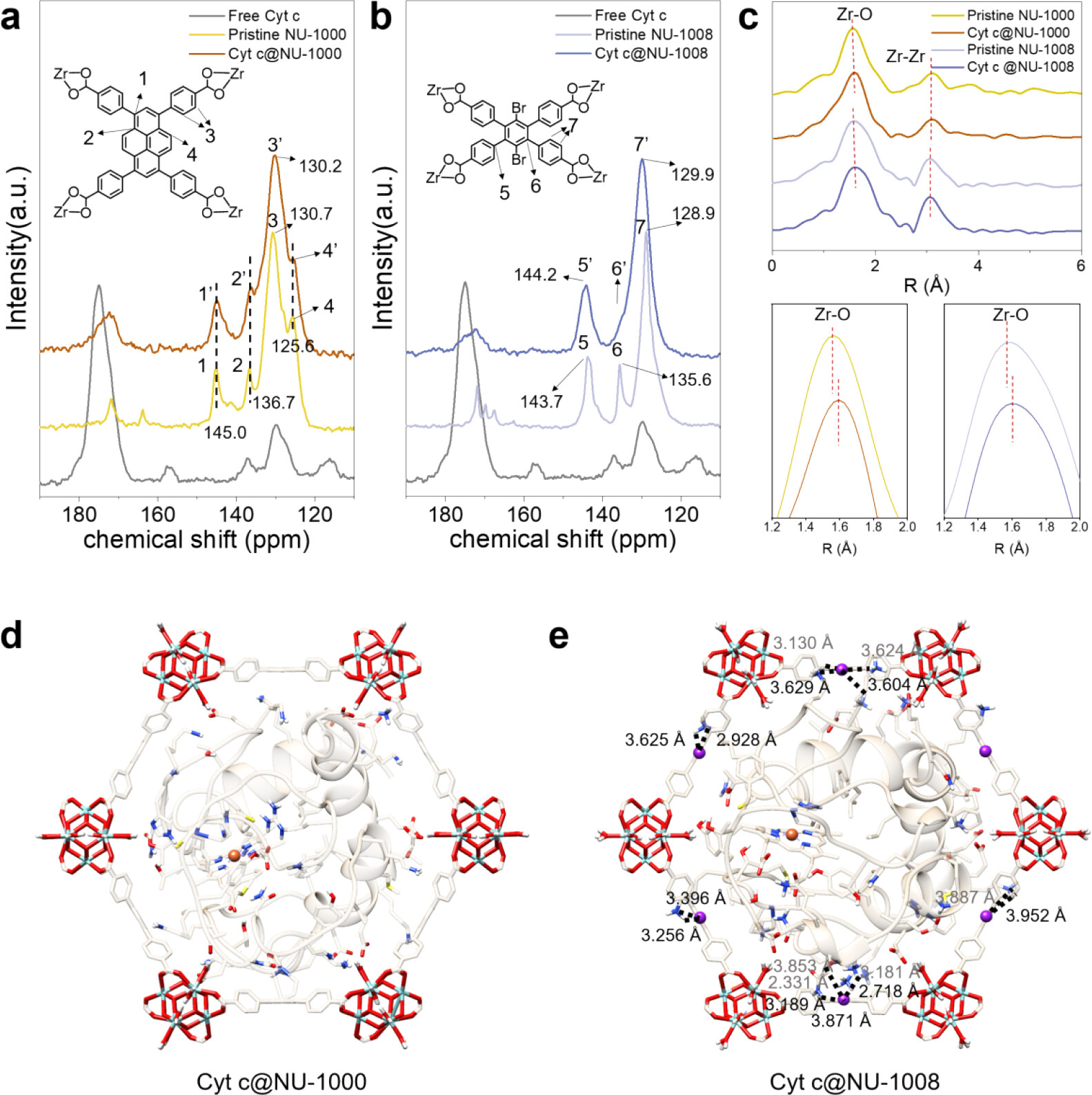
3. 谱学与自旋态:ESR证实Cyt c@NU-1000血红素铁为五配位高自旋(S=3/2),Cyt c@NU-1008为四配位高自旋(S=5/2);EXAFS显示酶负载后Zr-O键伸长,Zr-Zr键不变,Zr-O配位键扭曲;XPS证实Zr 3d结合能降低,配位键弱化。
4. 稳定性与膜性能测试:Cyt c@NU-1000在pH=2.5、60℃条件下保留高活性,室温储存30天仍有65%活性;连续流膜60 h运行后结构完整,无酶泄漏,SMX去除率稳定>99%。
机理分析
1. 核心机理围绕主客体相互作用介导孔道自适应形变展开,NU-1000非极性配体与Cyt c作用力弱,孔道被动扩张,削弱Met80与血红素铁配位,形成高活性五配位Fe(S=3/2);2. NU-1008极性溴取代配体与Cyt c形成强偶极作用,配体弯曲导致孔道收缩,His18与Met80均脱离Fe中心,形成低活性四配位Fe;
3. DFT计算表明,五配位Fe的O-O键裂解无活化能垒(ΔG=-0.17 eV),高效生成Fe(IV)=O活性中间体,四配位Fe活化能垒高达0.65 eV,催化活性显著降低;同时,MOF纳米片的限域环境保护酶结构,提升极端条件下稳定性。
总结
1. 开发了普适的MOF纳米片制备方法,或可应用在其他MOF材料的纳米片制备中。有望大大增强MOF材料纳米片掺杂制备复合材料的可行性
2. 成功构建同构MOF纳米片-酶复合催化剂,首次可视化证实孔道自适应形变行为,揭示极性介导的形变-酶活性构效关系,实现酶活性数量级提升,开发长效催化膜并验证水污染治理实用性,革新酶固定化载体设计理念。
文章标题:Adaptive Pore Deformation in Metal–Organic Framework Nanosheets for Enhanced Enzymatic Catalysis
文章作者:Huasheng Yang, Ying Liu, Ziyang Cai, Yuhong Lin, Yong Shen, Xiaohui Liu, Yujian Shen, Linjing Tong, Tong Wu, Wei Huang, Hang Xing, Fang Zhu, Siming Huang, Guosheng Chen*, Lingmei Liu*, Yu Han*, Gangfeng Ouyang*
DOI:10.1021/jacs.5c22730
原文链接:https://pubs.acs.org/doi/10.1021/jacs.5c22730
本文为科研用户原创分享,用于学术宣传交流,具体细节请查阅原文。如有错误、侵权,请联系修改删除,未经允许不得复制转载。




