首页 >
行业动态 > 细胞内原位合成共价有机框架用于触发铁死亡及免疫治疗
细胞内原位合成共价有机框架用于触发铁死亡及免疫治疗
摘要:
澳门大学王瑞兵教授团队发表的研究(Adv. Mater.,DOI: 10.1002/adma.202510663)中,首次建立溶酶体内酸性催化亚胺缩合的结晶聚合策略,在活肿瘤细胞溶酶体中原位合成共价有机框架(COFs,命名为 UMCOF1)。该材料具备本征荧光与规整晶体结构,可实时示踪合成过程;其在溶酶体内形成会破坏溶酶体稳态、活化溶酶体铁离子,触发免疫原性铁死亡,显著增强体内抗肿瘤免疫治疗效果。该方法无需高温、有机溶剂与严苛无氧条件,在水相温和条件下即可实现 COFs 合成,为活细胞内治疗性聚合反应开辟新方向。
研究背景:
1. 行业问题:活体内合成非天然聚合物可调控细胞功能,但细胞内原位合成COFs等结晶聚合物面临水环境干扰、结晶困难等挑战;细胞内复杂环境阻碍聚合,产物缺乏结晶度,无法作为治疗工具,目前尚无相关报道。
2. 现有方案:人工聚合聚合物可用于生物应用,COFs因优势已应用于生物成像等领域,但传统溶剂热合成条件苛刻,无法在细胞内温和合成,未探索其细胞内合成及抗肿瘤应用。
3. 本文创新:提出溶酶体内酸催化结晶聚合策略,用生物相容性单体在细胞溶酶体内原位合成亚胺连接COFs;利用其荧光特性追踪聚合过程,首次将其与铁死亡、免疫治疗结合,实现体内抗肿瘤治疗。
实验部分:
1. 缓冲液中常规COFs合成:
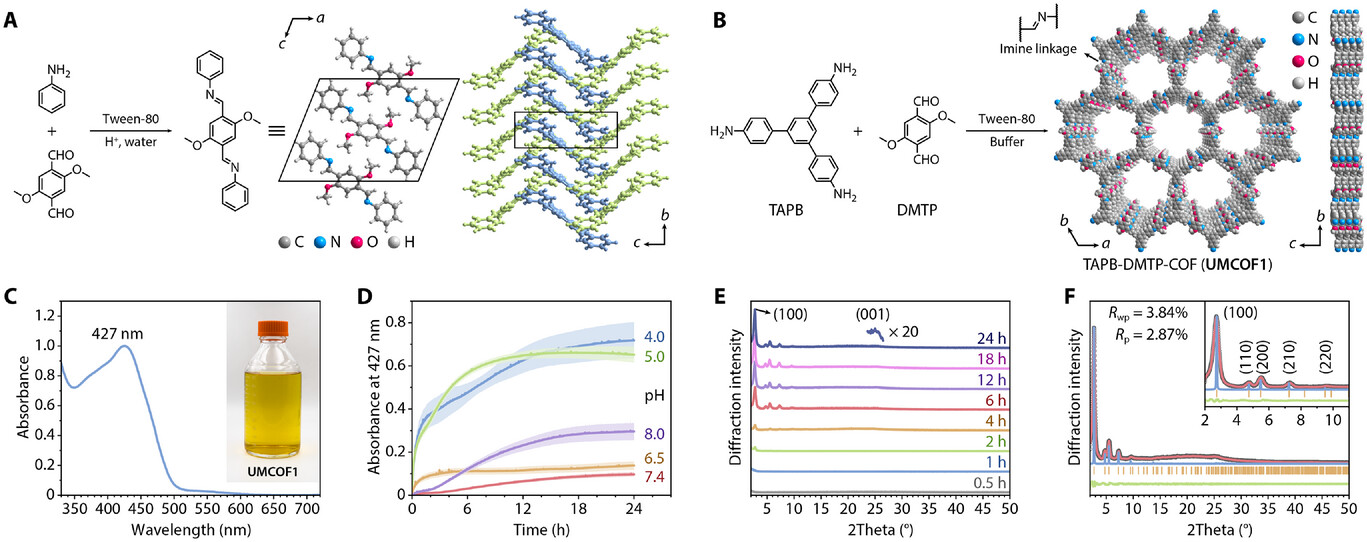
以苯胺与DMTP合成亚胺模型化合物(收率45%);TAPB与DMTP为单体,在10 mM、pH 5.0磷酸盐缓冲液中37℃合成UMCOF1(收率76%),还合成UMCOF2-UMCOF5(收率27%-66%),pH 4.0-5.0时聚合6 h达平衡,产物结晶性良好。
2. 细胞内原位合成TAPB-DMTP COF:
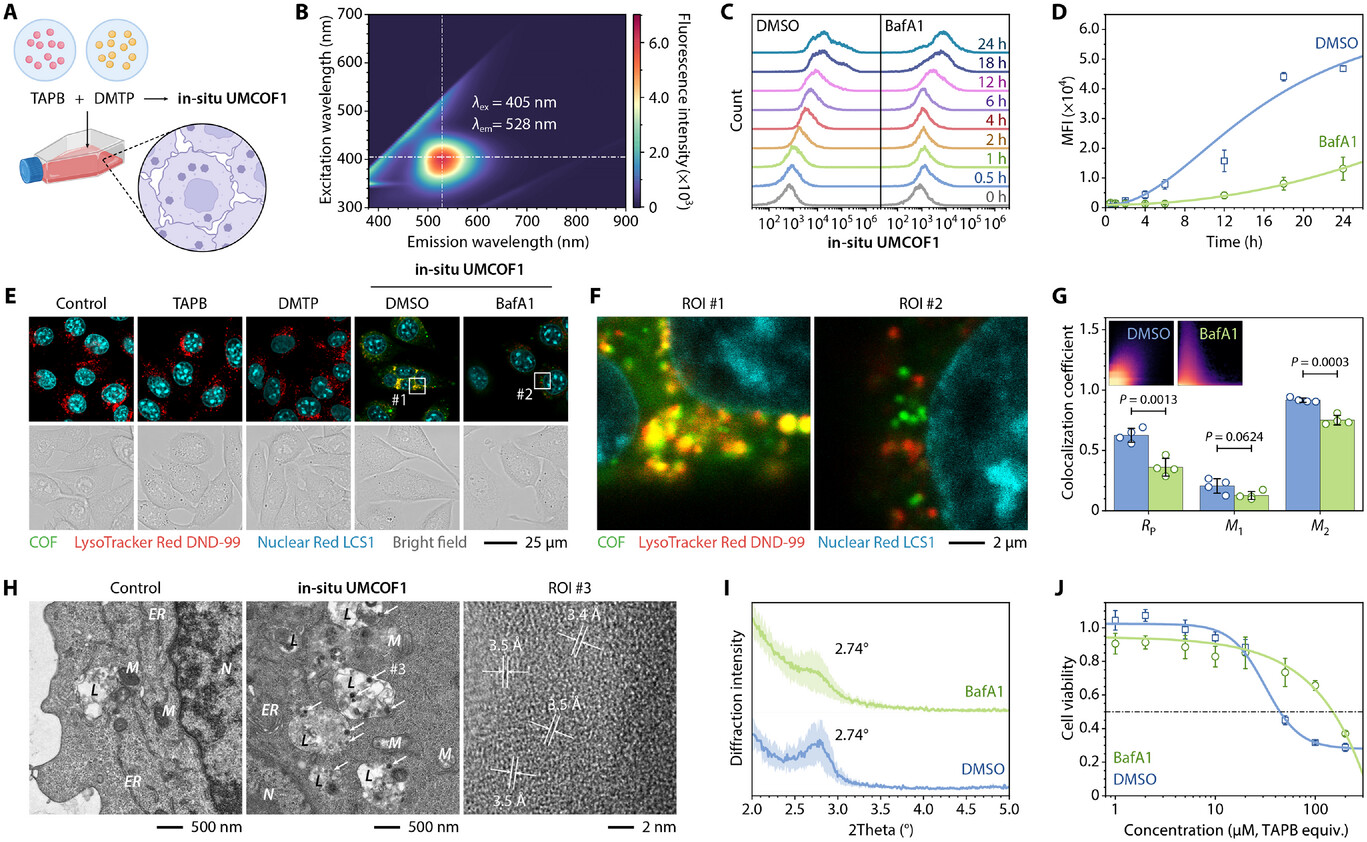
1) 以4T1细胞为模型,将TAPB(50 µM)与DMTP(75 µM)溶于含吐温-80的培养基中与细胞共孵育反应,利用溶酶体内酸催化结晶聚合,并通过流式细胞术、共聚焦显微镜等监测荧光变化;
2) 用巴氟霉素A1(BafA1)预处理抑制溶酶体酸化,观察荧光变化。结果表明,细胞内荧光随孵育时间递增,BafA1预处理使荧光强度降至28%;
3) 通过生物TEM、小角PXRD验证细胞内COFs的结晶性;COFs主要在溶酶体合成(Pearson相关系数0.626),粒径约120 nm,
4) 采用CCK-8法检测细胞活力,探究不同细胞系(CT26、MCF7等)及正常细胞的毒性差异。所得COF材料微粒对肿瘤细胞有细胞毒性(IC50约44.3 µM),对正常细胞也有一定毒性。
3. 铁死亡诱导:
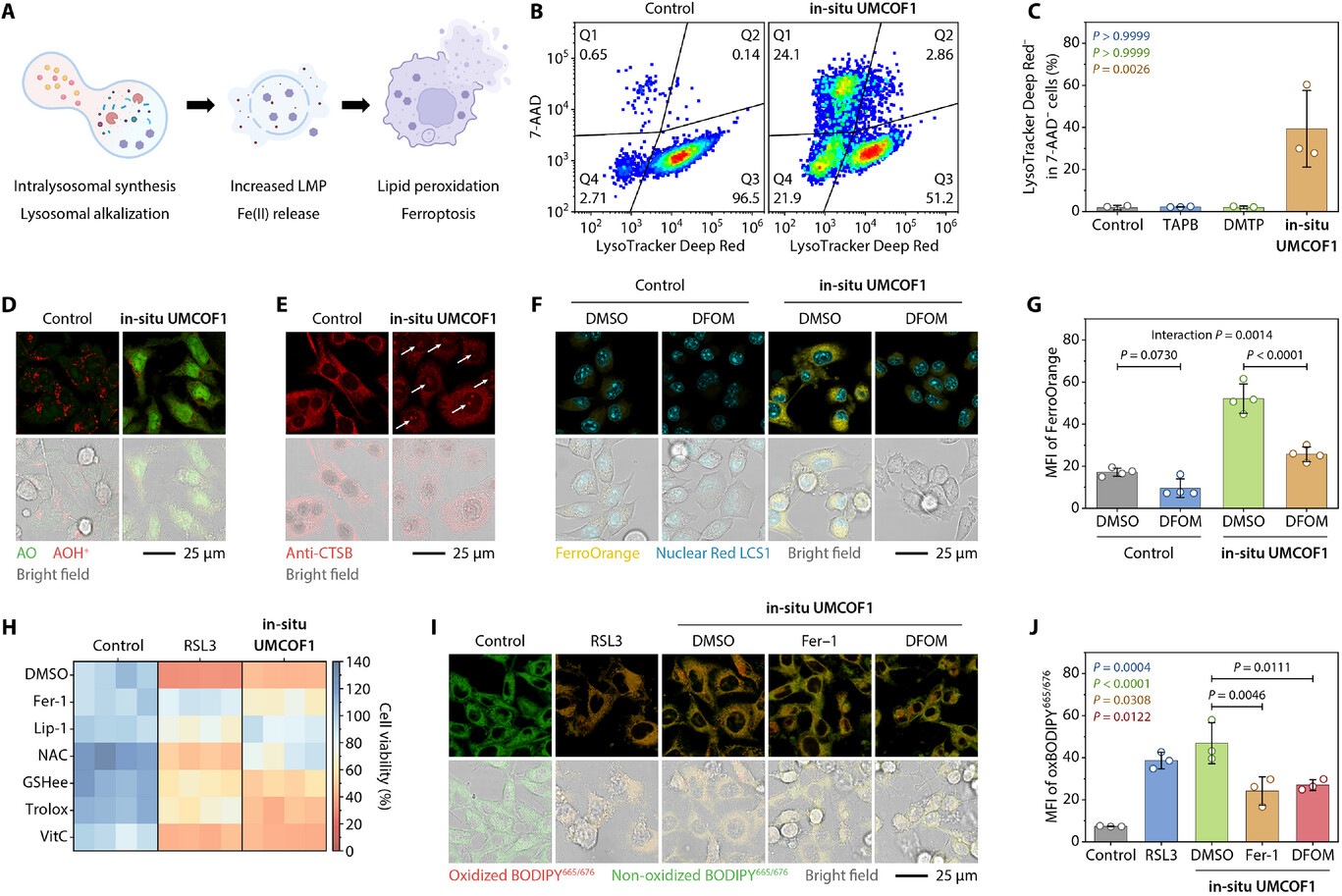
4T1细胞共处理后,诱导溶酶体碱化和膜通透性增加,胞内Fe(II)升高3倍,铁死亡抑制剂可拯救细胞,脂质过氧化显著升高,证实溶酶体介导的铁死亡。
4. 免疫原性及体内实验:
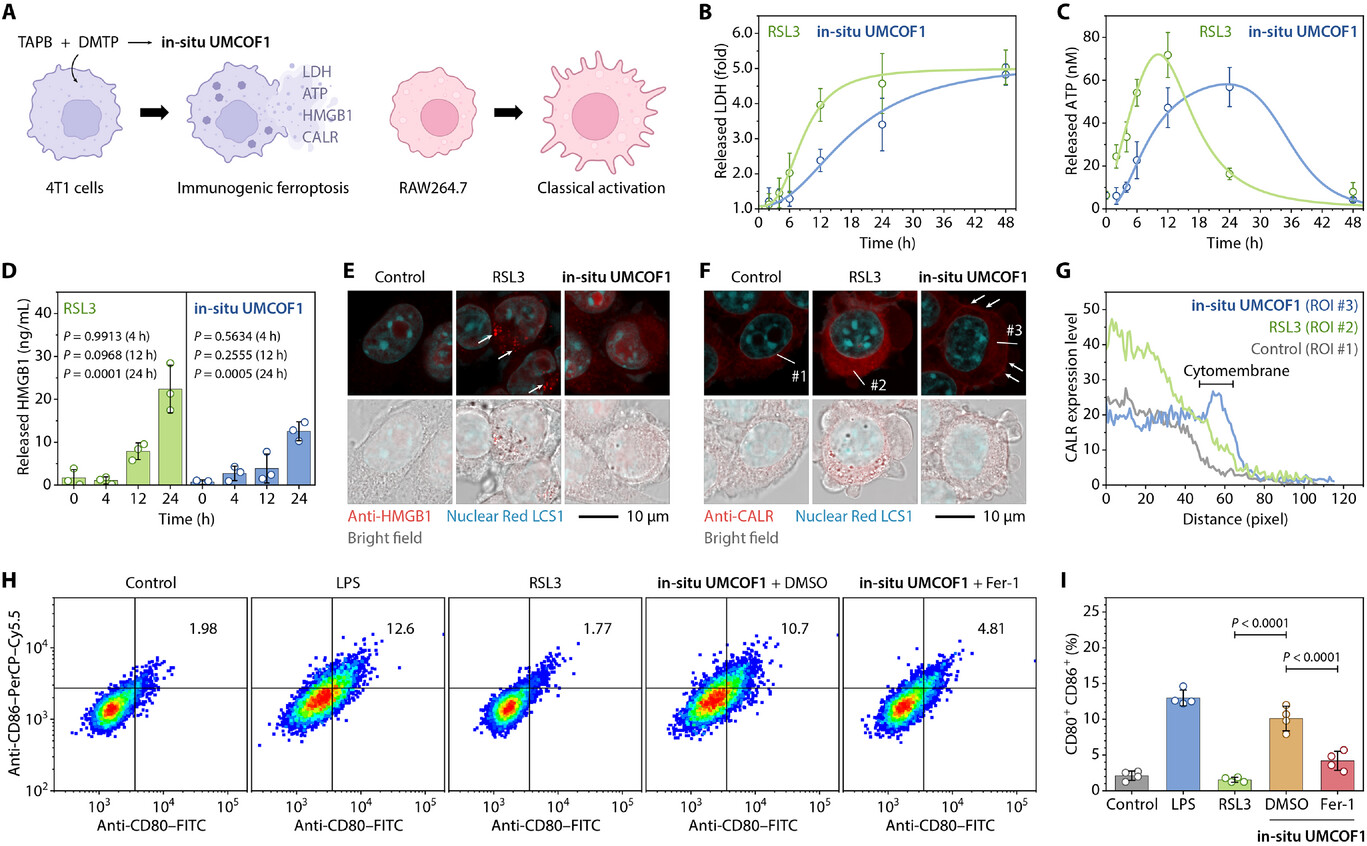
共处理诱导DAMPs持续释放,激活巨噬细胞和DC细胞;小鼠瘤内注射使肿瘤重量降至对照组19%,联合R848产生远位效应,肿瘤疫苗可预防BALB/c小鼠肿瘤形成。
实验突破:首次实现细胞内溶酶体原位合成结晶COFs,首次将其与免疫原性铁死亡结合,拓展COFs生物医学应用。
分析测试:
1. 结构与结晶性:UMCOF1为hcb网状、P3空间群,晶胞参数a=b=37.24 Å,c=3.53 Å,Pawley精修Rwp=3.84%、Rp=2.87%;细胞内COFs在2θ=2.74°有特征峰,HRTEM显示晶面间距3.5 Å,FT-IR验证亚胺键,TGA证实热稳定性。
2. 光学测试:UMCOF1可被405 nm激光激发,发射528 nm绿色荧光(寿命10.4 ns),最大吸收峰427 nm,pH 4.0-5.0聚合最快。
3. 细胞与体内表征:COFs与溶酶体共定位,BafA1预处理降低共定位;生物TEM观察到120 nm球形颗粒;小鼠瘤内注射后肿瘤损伤明显,GSH下降、MDA升高,IL6和TNFα升高,脾脏DC细胞增加4.9倍。
机理分析:
1. 细胞内原位合成COF机理:
依赖溶酶体酸性环境(pH 4.5-5.0),TAPB与DMTP经酸催化亚胺缩合、π-π堆积形成COFs,吐温-80促进单体溶解和摄取,BafA1预处理降低合成效率。
2. COF诱导铁死亡机制:
COFs形成及质子化导致溶酶体碱化、膜通透性增加,释放Fe(II)升高LIP,引发脂质过氧化,降低GSH、抑制GPX4,触发铁死亡,与传统诱导剂起源不同。
3. 免疫及抗肿瘤机理:
铁死亡导致细胞膜损伤,持续释放DAMPs,CALR膜表达是免疫原性关键;激活巨噬细胞和DC细胞,促进CD8+T细胞活化,联合R848产生远位效应,疫苗通过激活T细胞预防肿瘤。
总结:
1. 建立溶酶体内酸性催化原位结晶聚合新方法,首次在活细胞与肿瘤内合成结晶型 COFs,材料具备荧光示踪与规整结构。
2. 揭示溶酶体 COFs 合成→溶酶体损伤→铁离子释放→免疫原性铁死亡的完整机制,明确新型铁死亡途径。
3. 实现单体瘤内注射原位治疗,显著抑制肿瘤生长,联合免疫佐剂产生远端效应,可制备肿瘤疫苗,系统安全性良好。
4. 本研究为生物体催化COF合成提供新思路,打开了生物合成二维高分子聚合物的新窗口。
文章标题:In Situ Synthesis of Covalent Organic Frameworks Inside Cells for Triggering Ferroptosis and Immunotherapy
文章作者:Qun Guan, Le-Le Zhou, Zhiqing Yang, Yan-An Li, Leyong Wang, Ruibing Wang
DOI:10.1002/adma.202510663
文章链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202510663
本文为科研用户原创分享,用于学术宣传交流,具体细节请查阅原文。如有错误、侵权,请联系修改删除,未经允许不得复制转载。



