首页 >
行业动态 > 【水溶性nanoMOFs】甲氧基聚乙二醇磷酸酯可控配位制备金属有机框架基药物载体
【水溶性nanoMOFs】甲氧基聚乙二醇磷酸酯可控配位制备金属有机框架基药物载体
摘要:
金属有机框架纳米颗粒(nanoMOFs)在生物医学应用中研究广泛,但存在合成步骤繁琐、需有毒试剂、溶液中纳米颗粒保质期有限等问题,限制其临床转化。本文提出用磷酸酯功能化甲氧基聚乙二醇(mPEG-PO₃)对nanoMOFs进行后合成修饰,结合冻干法形成可再分散固体材料。该方法可简便储存裸nanoMOFs或载药nanoMOFs,所得PEG化nanoMOFs流体动力学直径稳定、胶体稳定性提升、药物释放动力学延迟。体外实验证实其细胞内稳定性提高、药物释放能力延迟且细胞毒性更低,为药物递送纳米载体设计提供新方向。
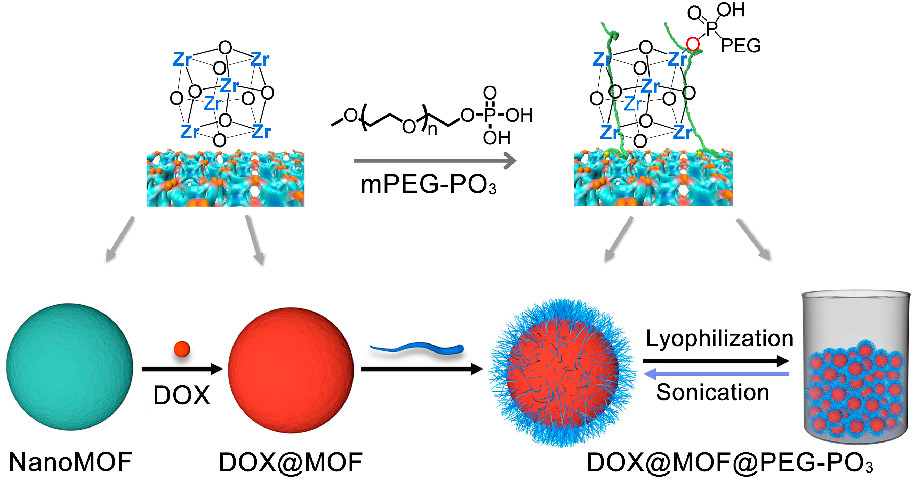
研究背景:
(1)行业问题和研究现状
- 行业问题:nanoMOFs用于生物医学时,功能化常需复杂合成方法、昂贵试剂或有毒催化剂,且多数nanoMOFs药物载体干燥后无法再分散,需保持溶液悬浮态,存在长期聚集和药物释放问题,保质期有限,阻碍临床转化。
- 研究现状:已有多种基于连接体或节点的共价/配位修饰策略,如用CuI催化UiO-66与PEG功能化、基于芳基自由基接枝分子到nanoMOFs表面、用磷脂双层保护卟啉nanoMOFs等,但存在各自局限。
(2)本文创新
在温和条件下,用mPEG-PO₃对Zr基nanoMOFs进行PEG化修饰,结合冻干法,解决nanoMOFs干燥后难再分散问题;揭示PEG化两步过程,且该方法适用于多种Zr基nanoMOFs,提升其稳定性和药物控释能力。
实验部分:
1.mPEG-PO₃合成:在0℃火焰干燥双颈烧瓶中,加POCl₃(100 mmol)的干燥DCM溶液和三乙胺(300 mmol),30分钟内加聚乙二醇甲醚(Mn=5000,30 mmol)的干燥DCM溶液,室温搅拌10小时,加水反应3小时,真空除DCM,透析(MWCO 3500)后冻干,得白色固体mPEG-PO₃(产率85%)。
2.Zr基nanoMOFs合成:如PCN-222,将TCPP(22.5 mg)、Zr₆簇(38 mg)、8 mL DMF和不同量TFA超声溶解,120℃加热5小时,离心(15000 rpm,35分钟),DMF洗3次、乙醇洗3次,得不同尺寸PCN-222(如117.8±12.9 nm);其他如UiO-66、MOF-808等合成方法类似,仅原料和反应条件略有差异。
3.PEG化nanoMOFs制备:将mPEG-PO₃水溶液(25 mg/mL,10 mL)加入nanoMOFs水悬浮液(10 mg/mL,5 mL),室温搅拌16小时,离心去未反应mPEG-PO₃,水重分散后透析(MWCO 12000-14000)12小时,冻干(0.008 mBar,-70℃)得PEG化nanoMOFs。
4.载药实验:nanoMOFs水悬浮液(5 mg/mL,6 mL)加DOX水溶液(15 mg/mL,4 mL),室温搅拌48小时,离心(15000 rpm,35分钟),水洗3次得DOX@MOF;再按PEG化步骤处理得DOX@MOF@PEG-PO₃,DOX负载量如PCN-222为23.2 wt%,PEG化后降至15.5 wt%。
分析测试:
1.PXRD:PCN-222@PEG-PO₃保留结晶性,出现2θ=19.0°和23.2°新峰(PEG所致);其他PEG化nanoMOFs类似,证实结构稳定性。
2.N₂吸附-脱附:PCN-222 BET面积1151 m²/g,PEG化(16小时)后降至265 m²/g,N₂ uptake从526 cm³/g降至129 cm³/g;UiO-66@PEG-PO₃ BET面积292 m²/g,证实mPEG-PO₃部分堵塞孔隙。
3.DLS与zeta电位:PCN-222流体动力学直径118.0 nm,PEG化后129.7±0.9 nm;zeta电位从31.7 mV变为-43.9±1.2 mV,其他如PCN-128@PEG-PO₃ zeta电位亦变负,胶体稳定性提升。
4.XPS:PCN-222中Zr 3d₃/₂和3d₅/₂结合能184.4 eV和182.0 eV,PEG化后降至183.5 eV和181.1 eV,F 1s峰减弱,证实Zr-O-P键形成。
5.TGA:PCN-222@PEG-PO₃(16小时)中mPEG-PO₃负载量32.9 wt%,PEG化nanoMOFs热稳定性略低于原nanoMOFs。
6.体外实验:500 μg/mL时,PCN-222对HeLa细胞存活率低,PCN-222@PEG-PO₃存活率超80%;DOX@128@PEG-PO₃在5 μg/mL时,24小时后才出现半数细胞死亡,药物释放延迟。
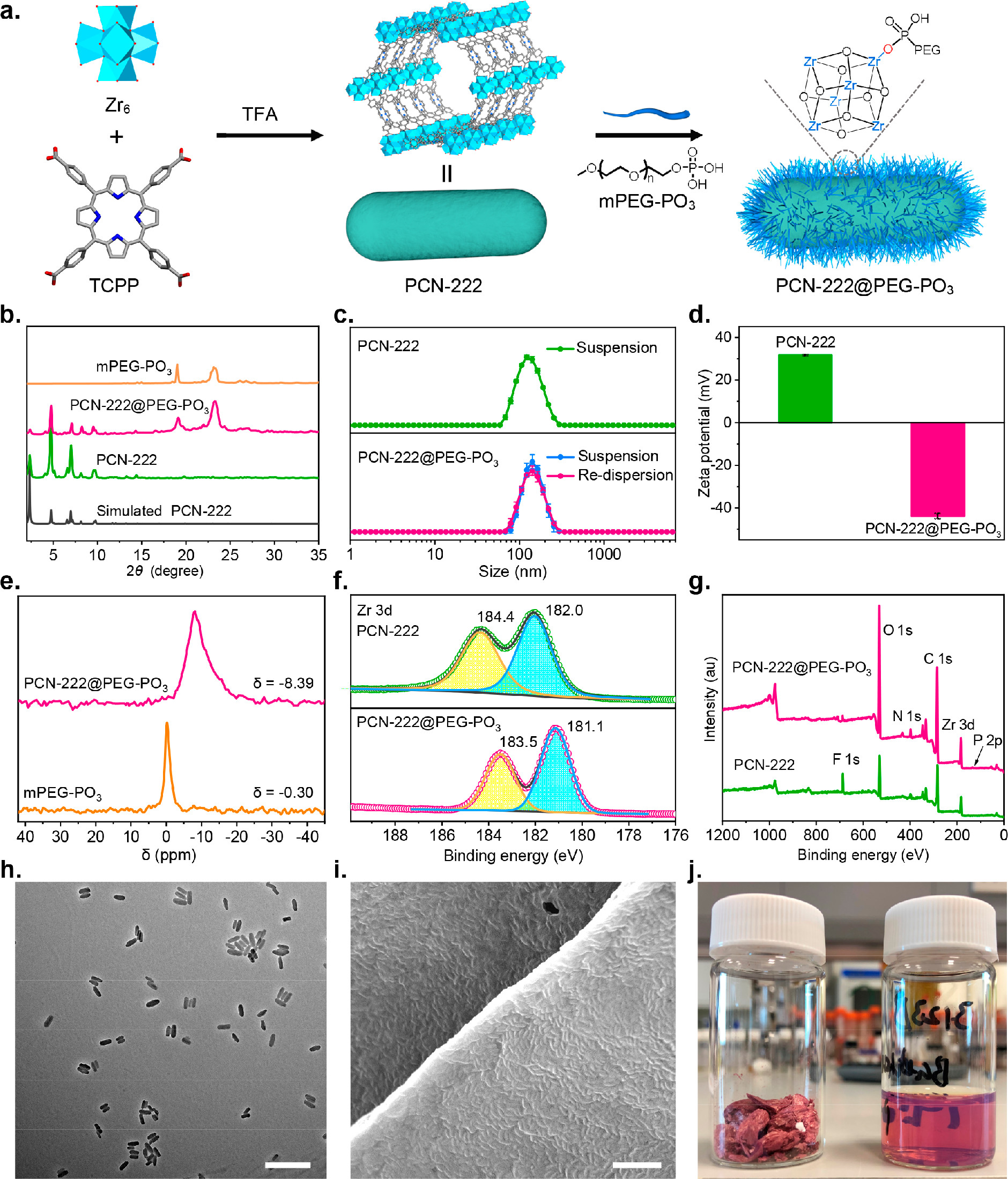
总结:
1.主要研究结果:实现多种Zr基nanoMOFs的PEG化修饰,所得材料可冻干再分散,胶体稳定性和细胞相容性提升,药物释放延迟。
2.创新突破:提出mPEG-PO₃可控配位修饰策略,揭示PEG化两步过程,解决nanoMOFs干燥后难再分散问题。
3.潜在意义:为MOFs基药物载体长期储存和临床转化提供新方法,推动其在药物递送领域应用。
Formulation of Metal−Organic Framework-Based Drug Carriers by Controlled Coordination of Methoxy PEG Phosphate: Boosting Colloidal Stability and Redispersibility
文章作者:Xu Chen, Yunhui Zhuang, Nakul Rampal, Rachel Hewitt, Giorgio Divitini, Christopher A. O’Keefe, Xiewen Liu, Daniel J. Whitaker, John W. Wills, Ravin Jugdaohsingh, Jonathan J. Powell, Han Yu, Clare P. Grey, Oren A. Scherman, David Fairen-Jimenez
DOI:10.1021/jacs.1c03943
文章链接:https://pubs.acs.org/doi/10.1021/jacs.1c03943
本文为科研用户原创分享用于学术宣传交流,具体内容请查阅上述论文,如有错误、侵权等请联系修改、删除。未经允许第三方不得复制转载。

