首页 >
行业动态 > 【HOF载药】氢键有机框架释放树突状细胞和T细胞活力用于靶向 CRISPR/Cas 辅助癌症免疫疗法
【HOF载药】氢键有机框架释放树突状细胞和T细胞活力用于靶向 CRISPR/Cas 辅助癌症免疫疗法
南京大学宋玉君等报道的本篇文章(Advanced Materials 2025, 2411886)中研究了一种微流控辅助合成的氢键有机框架(HOF)作为耗竭多胺的纳米平台,旨在释放树突状细胞(DCs)和 T 细胞的活力,用于精准癌症免疫疗法。该平台通过肿瘤细胞摄取后,负载的血浆胺氧化酶(PAO)能高效耗竭多胺,重塑肿瘤微环境并减轻 T 细胞免疫抑制。同时,该过程产生的丙烯醛和 H₂O₂ 触发 CRISPR 辅助新抗原生成,HOF 利用 CPPO-H₂O₂ 反应产生的能量实现单线态氧生产,从而裂解二硫键并释放 CRISPR-Cas9,敲除 DNA 错配修复相关基因 MLH1,进一步增加突变负担并产生新抗原,为 DCs 提供理想靶点。这种双重作用策略不仅纠正了 T 细胞免疫抑制,还增强了 DCs 的功效,为肿瘤免疫疗法提供了有力方法。
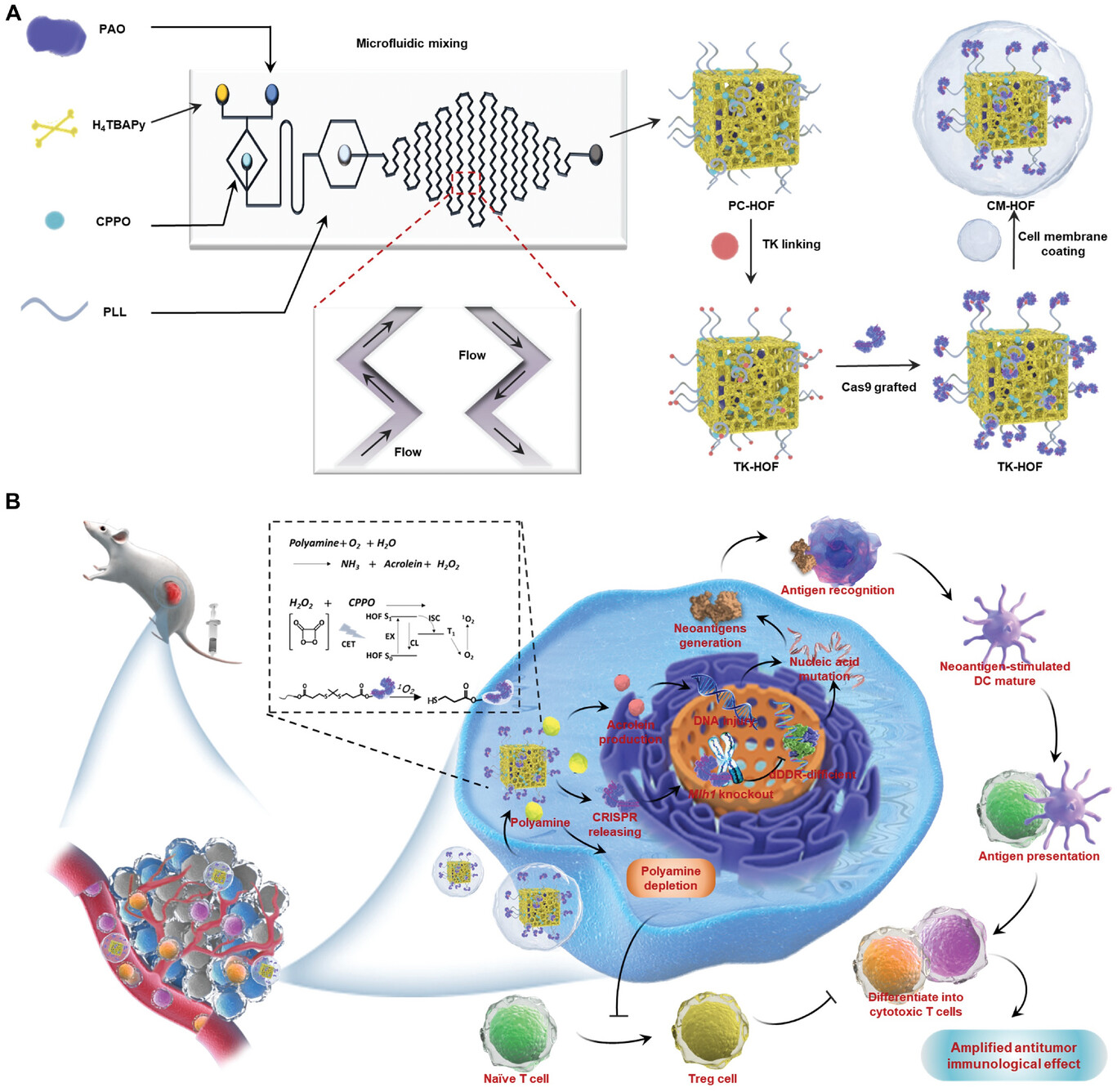
研究背景
1.行业问题
1) 传统的多胺代谢靶向治疗如 α-difluoromethylornithine 效果有限,需要更有效的策略。
2) DNA 错配修复(MMR)途径的调控在癌症免疫疗法中具有潜力,但如何有效干预该途径仍待探索。
3) CRISPR-Cas 基因编辑技术在递送和活性时空控制方面面临挑战。
2.研究现状
1) 其他学者尝试通过不同方法调节多胺代谢以抑制肿瘤生长,但效果不佳。
2) 针对 DNA MMR 途径的研究多集中在基因突变与癌症发生的关系上。
3) 在基因编辑递送系统方面,已有多种纳米材料被探索,但存在不足。
3.本文创新
1) 设计了一种微流控辅助合成的氢键有机框架(HOF)纳米平台,实现多胺耗竭与基因编辑的协同作用。
2) 创新性地将 PAO 和 CPPO 共封装于 HOF 中,并通过硫醚键连接 CRISPR 系统,利用肿瘤内源性多胺触发单线态氧生成,实现 CRISPR 的可控释放。
3) 通过肿瘤细胞膜包覆提高纳米平台的肿瘤靶向性。
实验和分析
1.材料合成与表征
1) 通过微流控芯片合成了负载 PAO 和 CPPO 的 PLL 稳定 HOF(PC-HOF),并用 FTIR 等验证了 CPPO 的负载。
2) 制备了硫醚修饰的 CPPO-HOF(TK-HOF),并通过碳二亚胺化学与 Cas9 蛋白连接,形成 Cas9-HOF。
3) 最终用癌细胞膜包覆,形成 CM-HOF,透射电镜(TEM)、粉末 X 射线衍射(PXRD)、氮气吸附-脱附等表征显示其具有良好的结晶结构和孔隙特性,且在不同溶液中稳定性良好。
2.应用性能测试
1) 在体外实验中,CM-HOF 对多种癌细胞表现出良好的细胞摄取能力和细胞毒性,能有效诱导细胞凋亡。
2) 通过流式细胞术等检测,CM-HOF 能促进 DCs 的成熟和 T 细胞的活化,增加细胞毒性 T 细胞比例,减少免疫抑制细胞 Treg 的数量,并上调免疫相关细胞因子的分泌。
3) 在体内抗肿瘤实验中,CM-HOF 对 CT26 肿瘤模型表现出显著的抑制效果,肿瘤生长明显减缓,肿瘤细胞凋亡增加,且具有良好的生物安全性。
3.性能原因分析
1) HOF 的多孔微环境有利于物质的扩散和反应,PAO 能高效耗竭肿瘤内的多胺,产生 H₂O₂ 和有毒的丙烯醛,后者诱导 DNA 损伤,同时 2) H₂O₂ 与 CPPO 反应生成单线态氧,裂解二硫键释放 CRISPR-Cas9,敲除 MLH1 基因,进一步增强 DNA 损伤和免疫原性。
3) 癌细胞膜包覆提高了纳米平台的肿瘤靶向性,减少了非特异性清除。
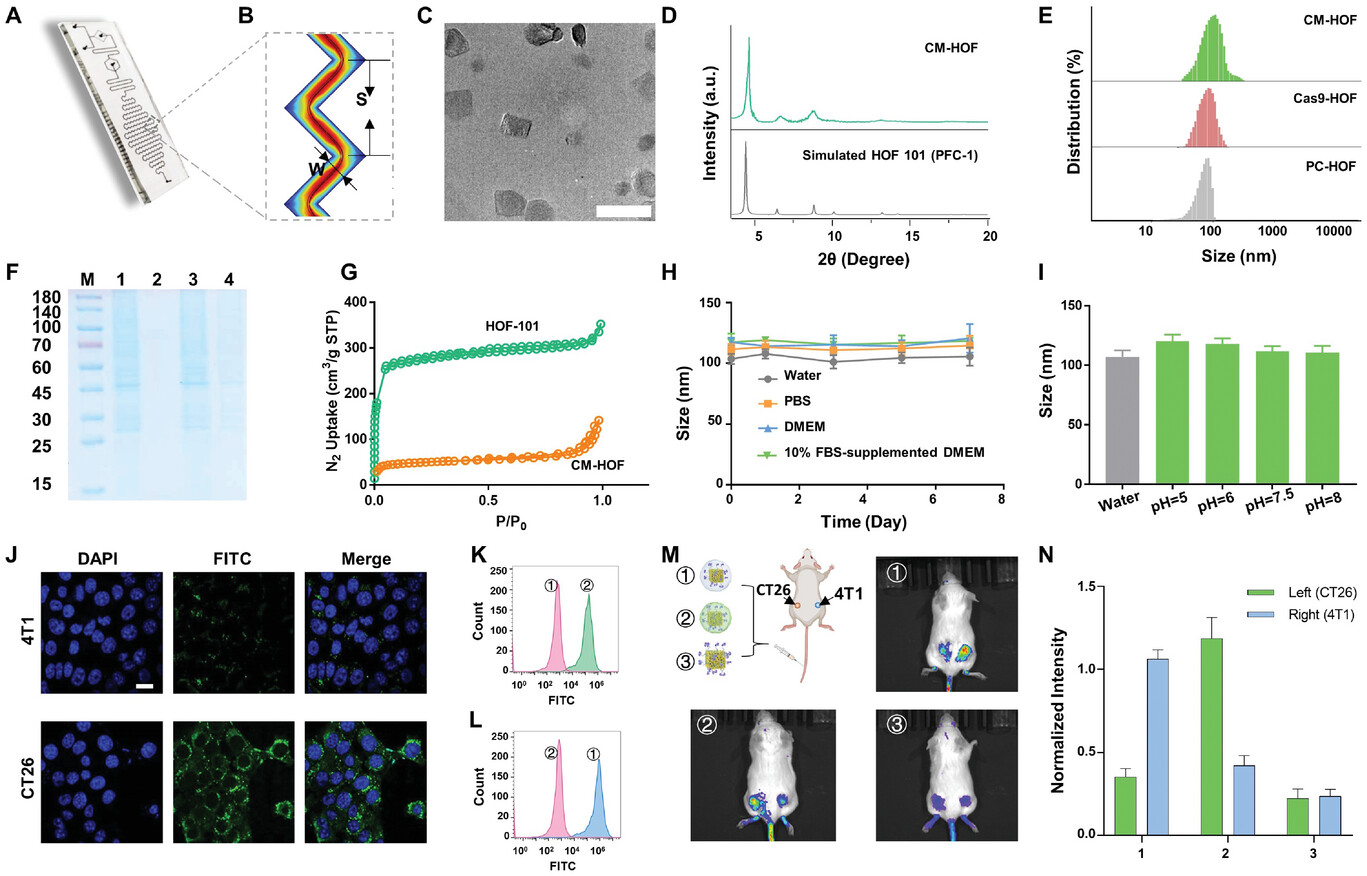
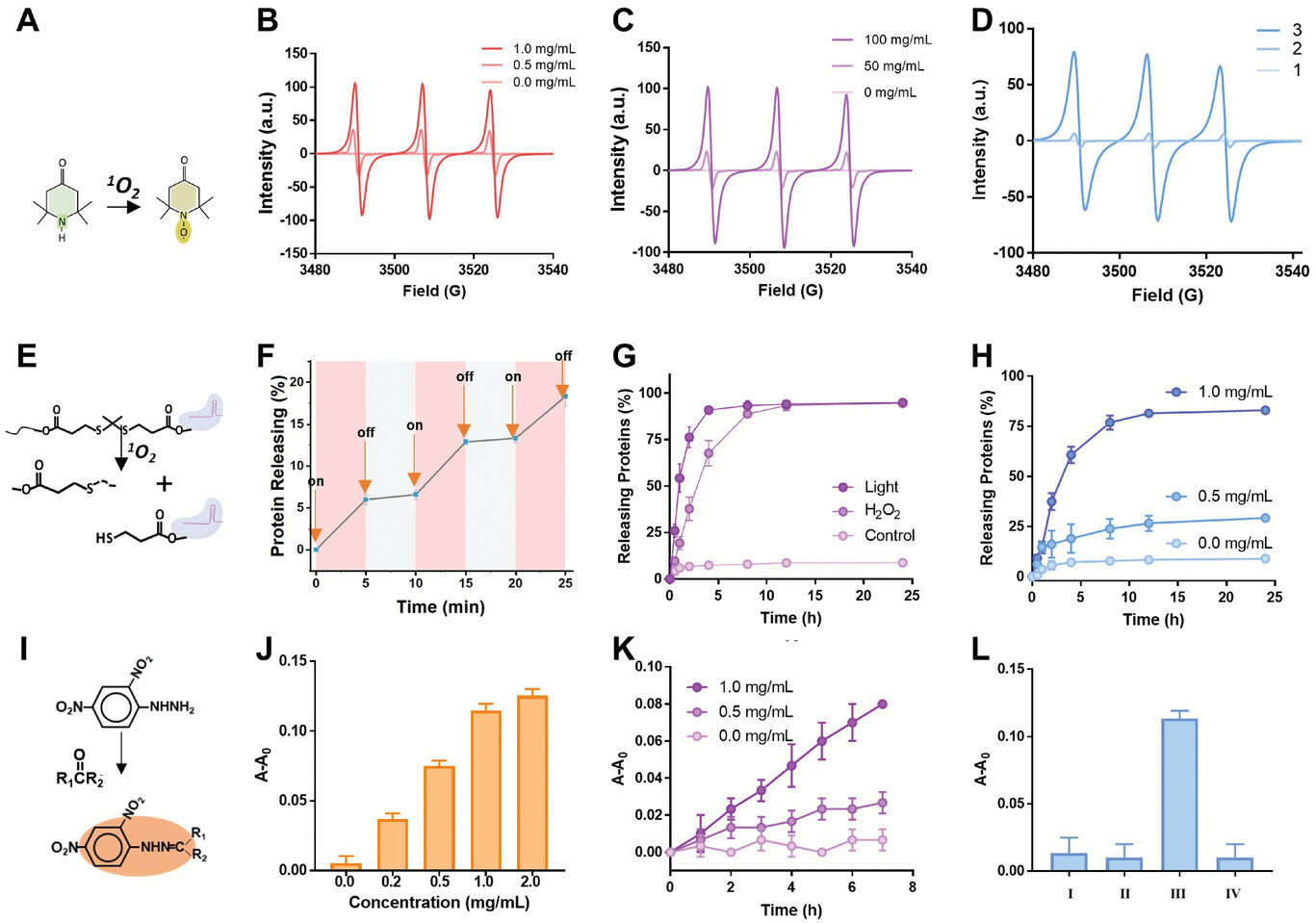
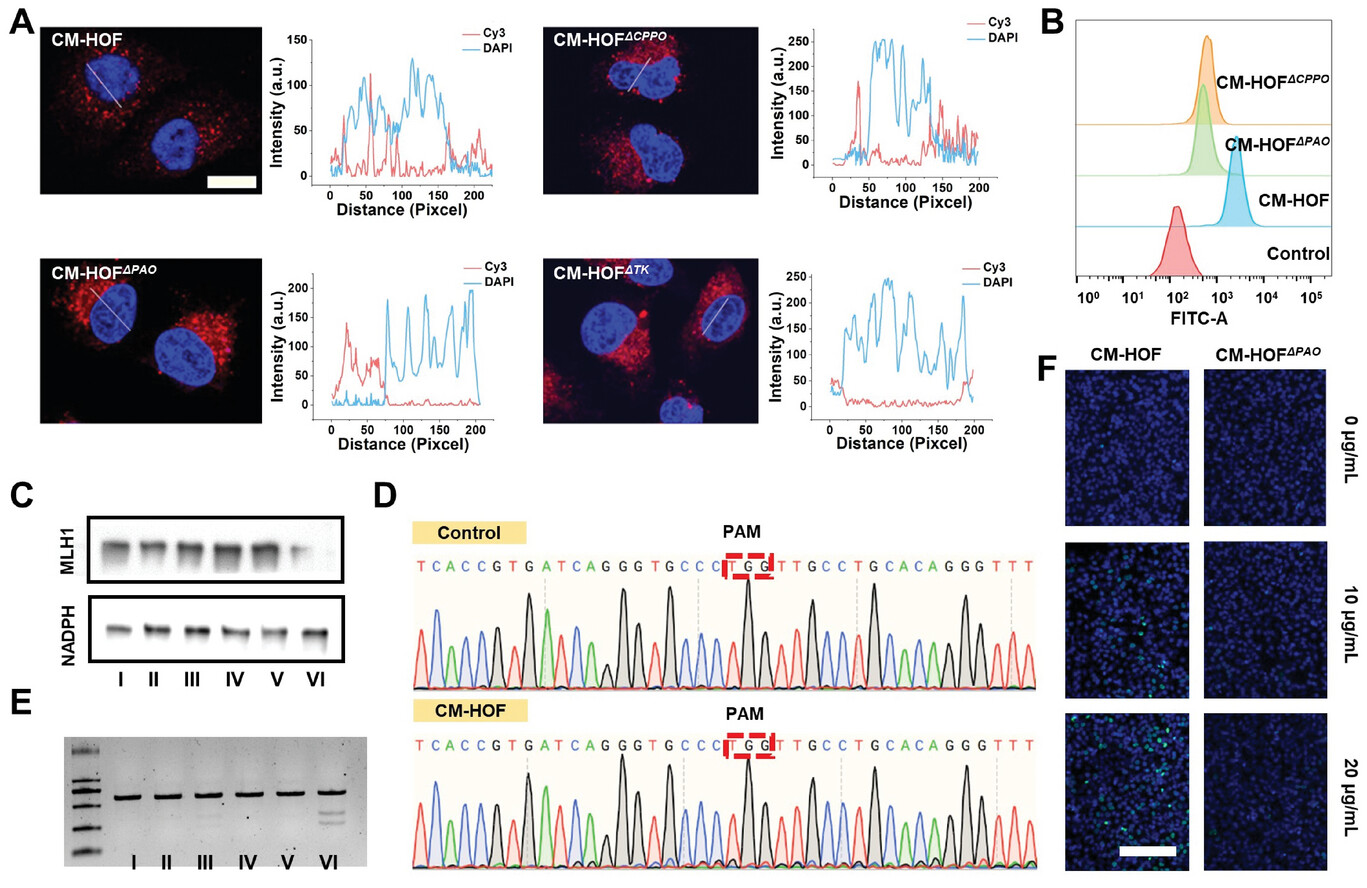
总结
1.成功设计并制备了一种微流控辅助合成的氢键有机框架纳米平台(CM-HOF),实现了多胺耗竭与基因编辑的协同作用,有效激活了树突状细胞和 T 细胞,增强了抗肿瘤免疫反应,在体内外实验中均表现出良好的抗肿瘤效果和生物安全性。
2.创新性地将多胺耗竭与 CRISPR 基因编辑相结合,利用肿瘤内源性多胺触发单线态氧生成实现基因编辑系统的可控释放,为癌症免疫疗法提供了新策略。
3. 通过微流控技术和癌细胞膜包覆提高了纳米平台的合成精度和肿瘤靶向性。
4. 为氢键有机框架材料在生物医学领域的应用提供了新的实例,拓展了其应用范围。
Polyamine-Depleting Hydrogen-Bond Organic Frameworks Unleash Dendritic Cell and T Cell Vigor for Targeted CRISPR/Cas-Assisted Cancer Immunotherapy
文章作者:Yongchun Pan, Fei Zeng, Xiaowei Luan, Guanzhong He, Shurong Qin, Qianglan Lu, Bangshun He, Xin Han, Yujun Song
DOI:10.1002/adma.202411886
文章链接:https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202411886
本文为科研用户原创分享用于学术宣传交流,具体内容请查阅上述论文,如有错误、侵权等请联系修改、删除。未经允许第三方不得复制转载。



