首页 >
行业动态 > 【TAPP-APA COF】缺氧激活的可生物降解卟啉基COF材料用于伤口感染的光动力和光热治疗
【TAPP-APA COF】缺氧激活的可生物降解卟啉基COF材料用于伤口感染的光动力和光热治疗
摘要:
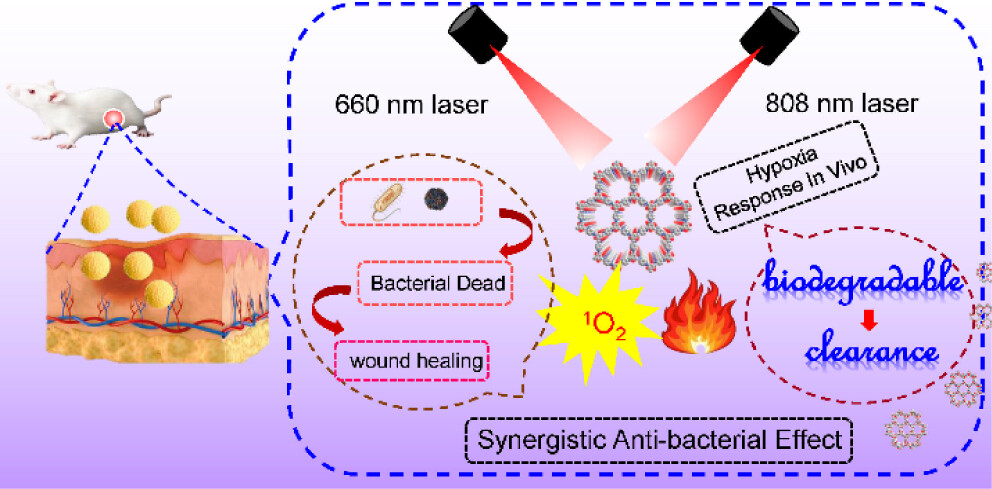
山西医科大学崔宏、张瑞平老师等报道的本篇文章(ACS Appl. Mater. Interfaces 2024)中介绍了一种新型的缺氧激活的可生物降解卟啉基共价有机框架(HRCOFs),用于创面感染的光动力治疗(PDT)和光热治疗(PTT)。HRCOFs含有卟啉骨架和缺氧敏感的偶氮苯基团,能够在660 nm激光照射下产生单线态氧(1O2),并在808 nm近红外激光照射下产生热能。体外实验显示HRCOFs对金黄色葡萄球菌(S. aureus)和大肠杆菌(E. coli)具有优异的协同抗菌能力。体内实验也证实了HRCOFs对创面感染具有协同PDT和PTT效果。重要的是,HRCOFs能够响应创面微环境,可降解并清除,避免了体内长时间滞留引起的不良反应,显示出良好的生物相容性。总体而言,这种具有光动力和光热效应的可生物降解HRCOFs可以用于抗菌感染,并为促进创面愈合提供了重要价值。
研究背景:
1)创面感染已成为人类健康的主要威胁之一,抗生素的滥用导致耐药细菌的发展,限制了原有抗菌治疗的效果。
2)银和其他金属离子显示出有效的抗菌效果,但其对哺乳动物细胞的严重毒性限制了它们的应用。天然抗菌化合物也被认为是治疗细菌感染的策略之一,但其低抗菌活性和效能限制了它们在替代合成抗生素中的应用。
3)本文作者设计并制造了含有卟啉分子和缺氧敏感偶氮键的缺氧响应性可生物降解卟啉基共价有机框架(HRCOFs),用于光动力和光热协同抗菌治疗。
实验部分:
1. HRCOFs的合成:
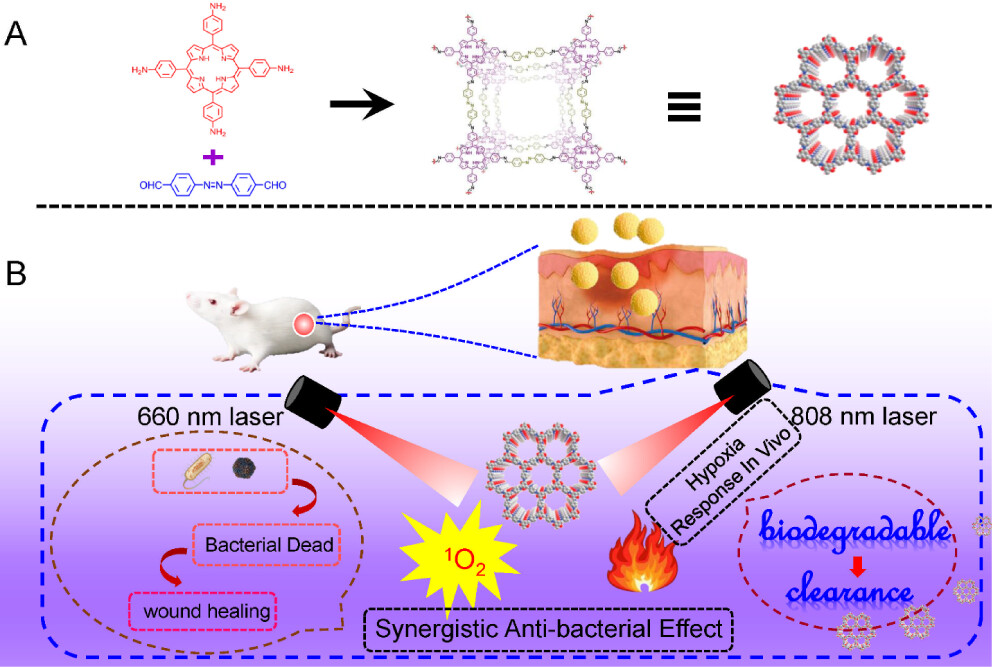
1) 将5,10,15,20-四(4-氨基苯基)卟啉(TAPP)和4,4'-偶氮二苯甲醛(APA)以1:2的摩尔比混合在9 mL四氢呋喃(THF)中,然后在暗处搅拌12小时。
2) 向上述溶液中加入200 μL三氟乙酸,继续在暗处搅拌12小时,之后通过离心收集产物,并用THF重悬,再次离心以去除未反应的单体。
3) 将收集的HRCOFs产物用去离子水和乙醇多次洗涤,最后在60 °C下真空干燥过夜,得到最终的HRCOFs粉末。
2. HRCOFs的缺氧响应性测试:
1) 将HRCOFs分散在10 mM PBS溶液(pH=7.4)中,并与2 mM的硫化钠(Na2S2O4)在37 °C下混合6小时。
2) 使用透射电子显微镜(TEM)和动态光散射(DLS)检测HRCOFs的形貌和尺寸变化。
3. HRCOFs的光动力性质测试:
1) 将1,3-二苯基异苯并呋喃(DPBF)和HRCOFs混合在DMF溶液中,使用660 nm激光(100 mW/cm²)照射,并实时监测DPBF在415 nm处的吸收变化。
2) 使用电子自旋共振(EPR)技术,以2,2,6,6-四甲基哌啶(TEMP)作为自旋陷阱剂,检测HRCOFs在660 nm激光照射下产生的单线态氧(1O2)。
4. HRCOFs的光热性质测试:
1) 将不同浓度的HRCOFs溶液(50, 100, 200, 300 μg/mL)用808 nm激光(1.0 W/cm²)照射5分钟,并使用红外热成像相机记录温度变化。
2) 将200 μg/mL的HRCOFs溶液用不同功率密度(0.25, 0.50, 0.75, 1.0 W/cm²)的808 nm激光照射,评估光热性能。
5. 抗菌活性测试:
1) 将S. aureus和E. coli与HRCOFs及激光照射处理,通过平板计数法评估抗菌效率。
2) 使用活/死细菌染色法(SYTO 9/PI)和共聚焦激光扫描显微镜(CLSM)观察细菌的存活情况。
3) 使用扫描电子显微镜(SEM)观察细菌的形态变化。
6. 体内抗菌治疗实验:
1) 建立S. aureus感染的小鼠创面模型,将小鼠随机分为五组,分别给予PBS、HRCOFs、HRCOFs+PDT、HRCOFs+PTT和HRCOFs+PDT+PTT处理。
2) 在预定时间点拍摄创面照片,使用ImageJ软件测量创面面积,并记录小鼠体重变化。
3) 治疗结束后,收集创面组织样本进行H&E和Masson三色染色,以及主要器官的H&E染色进行组织学分析。
分析测试:
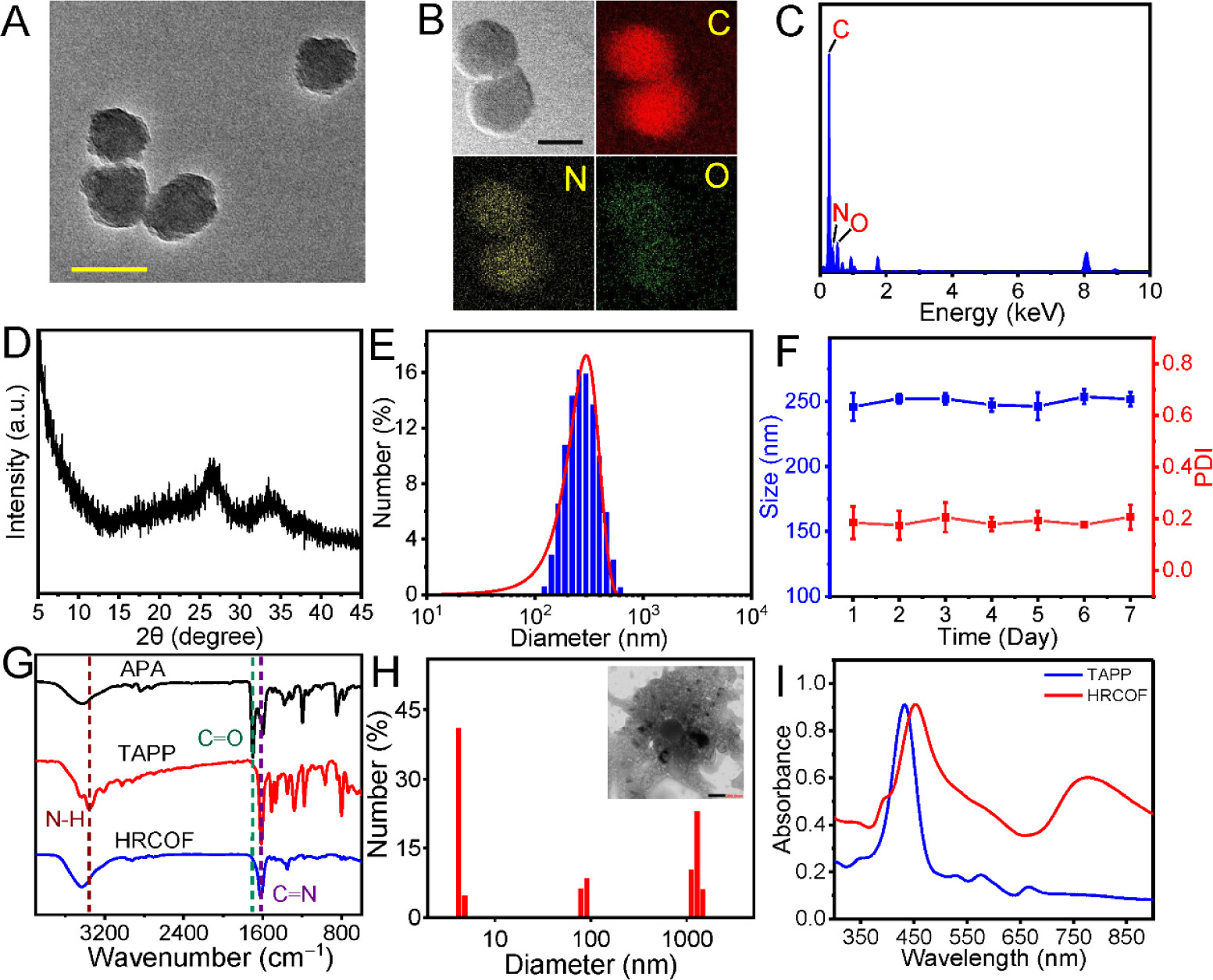
1. 样品形态学表征:使用透射电子显微镜(TEM)观察HRCOFs的形貌和尺寸,结果显示均匀球形形貌,平均粒径约为160 nm。
2. 元素分布和化学成分分析:通过能量色散X射线光谱(EDS)分析HRCOFs中的元素分布,确认了C、N、O等元素的存在。
3. 晶体性质分析:粉末X射线衍射(PXRD)结果显示HRCOFs在26.6°和34.04°处有两个峰,表明其非晶态结晶。
4. 化学键合分析:傅里叶变换红外光谱(FT-IR)显示HRCOFs中C=N键的出现和C=O、N-H键的消失,证实了席夫碱缩合反应的成功。
5. 粒径及稳定性分析:动态光散射(DLS)测量显示HRCOFs在水中的平均直径为250 nm,且在PBS溶液中具有优异的胶体稳定性。
6. 光物理性质分析:紫外-可见(UV-vis)光谱显示HRCOFs的Soret带和Q带与单体TAPP相比发生了红移,并且在NIR区域显示出广泛的吸收范围。
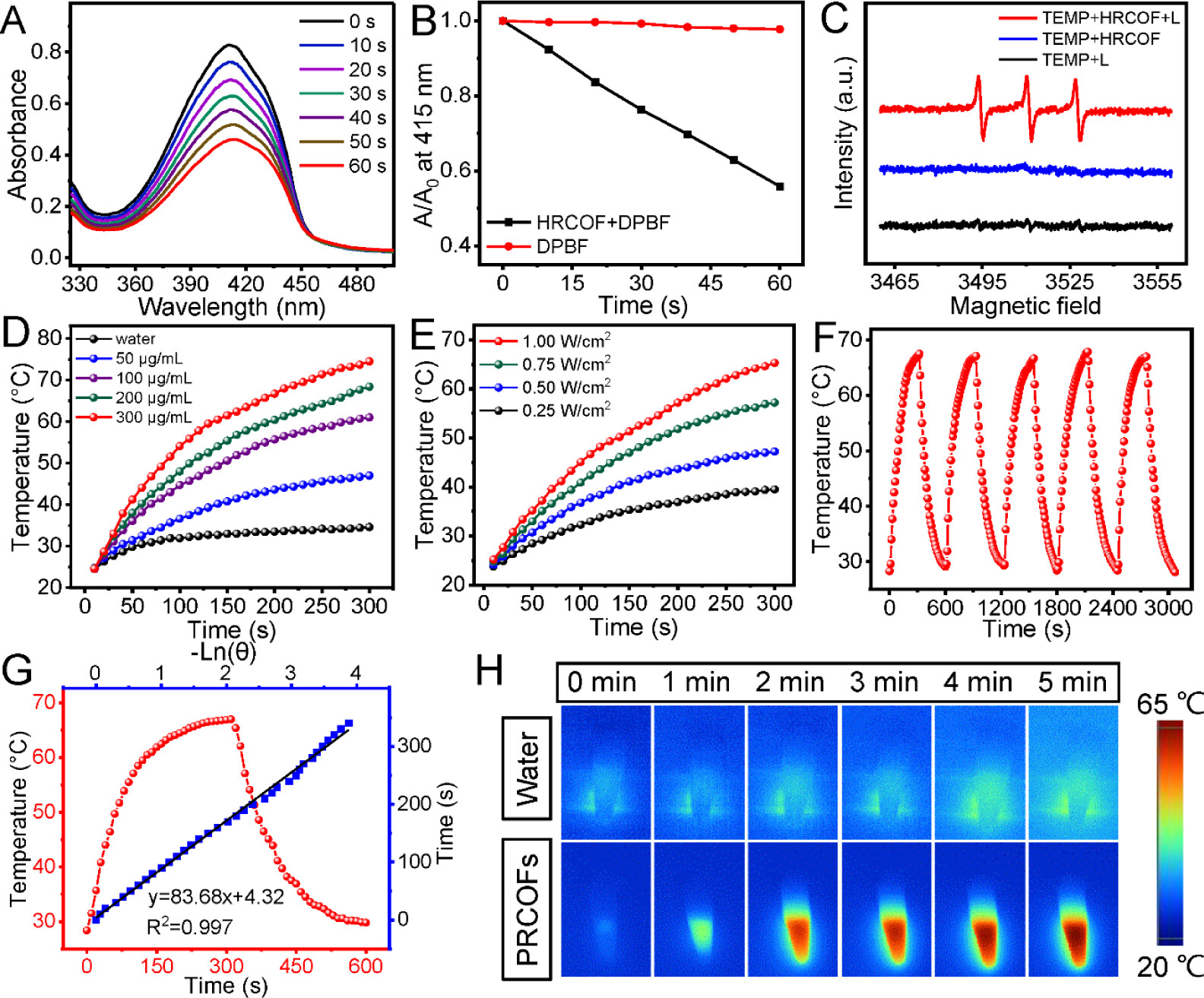
7. 单线态氧生成测试:DPBF的UV-vis光谱变化和EPR分析结果表明HRCOFs能够在660 nm激光照射下产生1O2。
8. 光热性能测试:不同浓度的HRCOFs溶液在808 nm激光照射下的温度变化表明,HRCOFs的光热效应与其浓度呈正相关,即使在50 μg/mL的低浓度下,温度也能从24.8升至47°C。
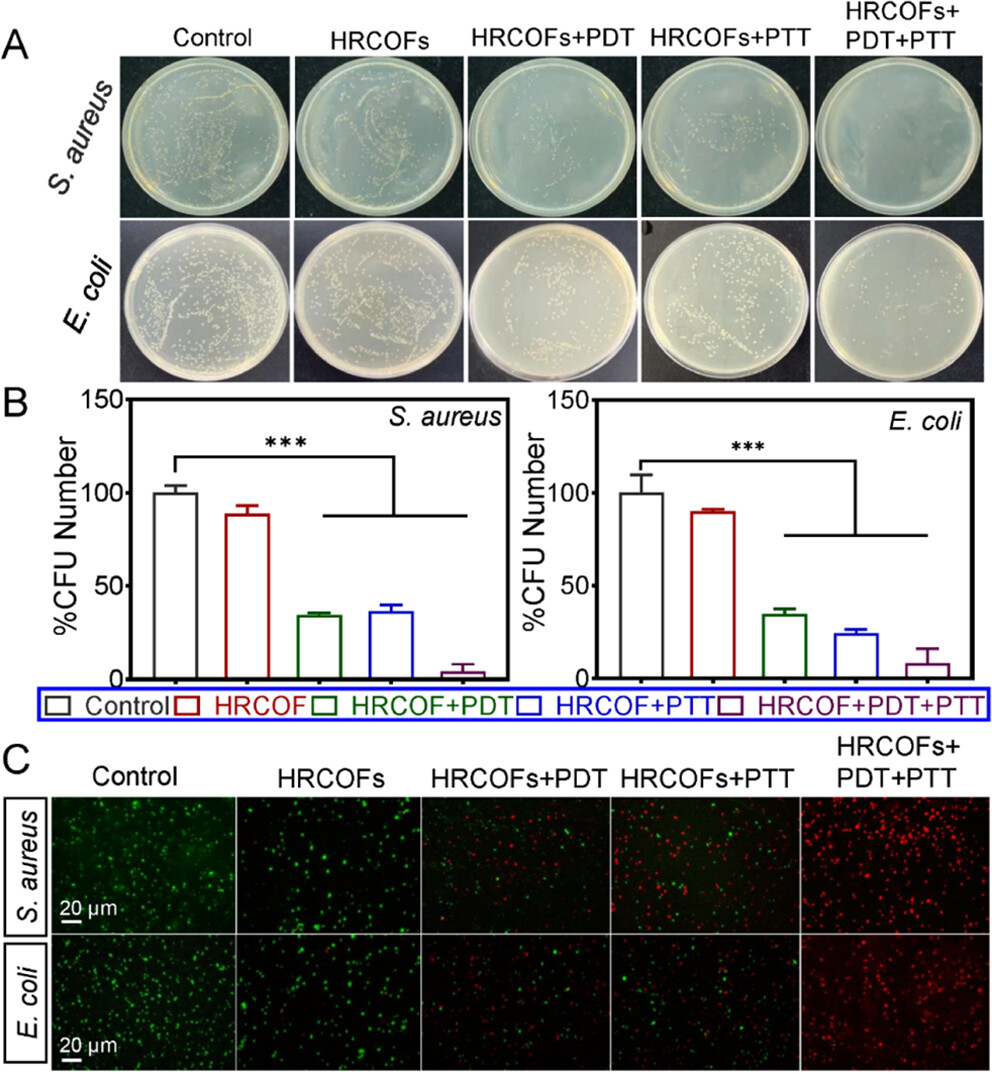
9. 抗菌效率测试:平板计数法结果显示,在HRCOFs存在下,经660 nm PDT或808 nm PTT激光照射后,S. aureus和E. coli的存活率显著下降,尤其是PDT+PTT组。
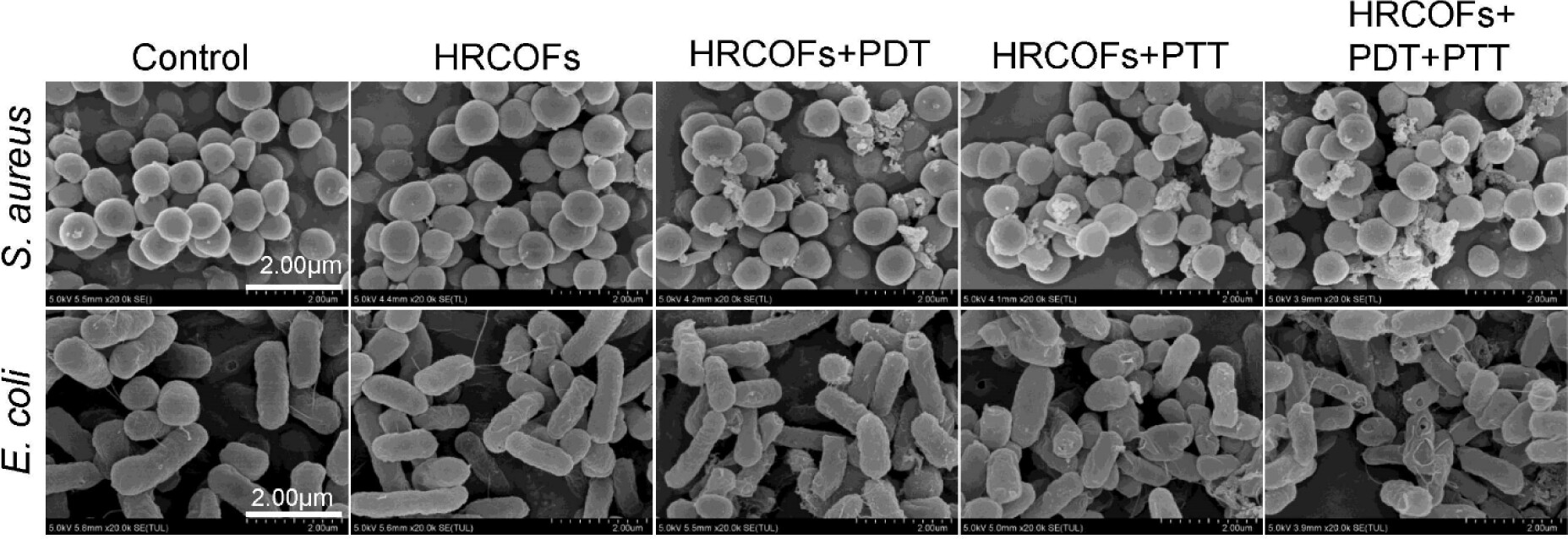
10. 细菌形态变化观察:SEM结果显示,经HRCOFs处理后的S. aureus和E. coli表面出现皱褶,PDT组因产生1O2而表面略微皱缩,PTT组因光热效应而表面略微变形,PDT+PTT组细胞壁粗糙且损伤更严重。
11. 体内抗菌治疗效果评估:小鼠创面模型实验结果显示,HRCOFs+PDT+PTT组的创面愈合效果最佳,创面面积最小,且残留细菌数量最少,表明HRCOFs具有良好的体内抗菌效果。
12. 生物相容性评估:通过CCK-8实验评估HRCOFs对L929细胞和NIH 3T3细胞的毒性,结果表明即使在高达400 μg/mL的浓度下,细胞活力仍高于90%,显示出良好的生物相容性。
13. 溶血活性测试:通过与不同浓度的HRCOFs混合的红细胞进行溶血实验,结果表明即使在高达400 μg/mL的浓度下,红细胞未出现明显溶血,表明HRCOFs具有良好的血液相容性。
总结:
本文成功制备了缺氧响应的可生物降解卟啉基共价有机框架(HRCOFs),在激光照射下产生单线态氧和热能,展现出PDT和PTT特性。体外实验表明HRCOFs对S. aureus和E. coli具有优异的协同抗菌效果。体内实验结果也证实了HRCOFs能够加速S. aureus感染创面的愈合,通过抗菌、毛囊恢复和胶原沉积。HRCOFs能够在缺氧微环境中被触发和降解,然后从体内清除。溶血和细胞毒性实验表明HRCOFs具有低毒性和良好的生物相容性。总之,HRCOFs为抗菌和创面愈合提供了一种新的策略和有前景的智能平台。
展望:
本文的科研成果为创面感染的治疗提供了新的思路和方法。未来研究中,作者可以进一步探索HRCOFs在不同类型创面感染中的应用效果,以及其在临床转化中的潜力。此外,可以研究HRCOFs的长期生物安全性和降解产物的代谢途径,以确保其在实际应用中的安全性。还可以探索HRCOFs与其他治疗手段(如抗生素、免疫疗法)的联合应用,以提高治疗效果。最后,可以研究HRCOFs在其他疾病治疗(如肿瘤治疗)中的潜在应用,拓宽其应用范围。
Hypoxia-Activated Biodegradable Porphyrin-Based Covalent Organic Frameworks for Photodynamic and Photothermal Therapy of Wound Infection
文章作者:Yulong Liu, Ya Li, Liqin Jiao, Yefang Kang, Baojie Du, Wenwen Cai, Hong Cui,* and Ruiping Zhang*
DOI:10.1021/acsami.4c14909
文章链接:https://pubs.acs.org/doi/10.1021/acsami.4c14909
本文为科研用户原创分享上传用于学术宣传交流,具体内容请查阅上述论文,如有错误、侵权等请联系修改、删除。未经允许第三方不得复制转载。





