首页 >
行业动态 > 【COF生物传感】:特定磁性共价有机框架限域的Os纳米酶团簇用于无干扰和超高灵敏度生物传感
【COF生物传感】:特定磁性共价有机框架限域的Os纳米酶团簇用于无干扰和超高灵敏度生物传感
摘要:
首都医科大学庞元凤&陈瑞和北京微生物与流行病学研究所肖瑞老师等报道的本篇文章(Adv. Funct. Mater.2024, 2400875)中开发了一种新型的磁性过氧化物酶(POD)模拟纳米酶,该纳米酶由共价有机框架(COF)限域的锇(Os)纳米团簇组成,命名为Fe3O4@COF@Os。这种纳米酶能够用于生物标志物的生物传感,特别是在现场快速诊断(POC)疾病诊断中。研究发现,通过改变还原剂和COF配体的功能基团,可以调节Fe3O4@COF@Os的催化活性和特异性。使用抗坏血酸作为还原剂和含氟的COF配体,Fe3O4@COF@Os展现出卓越的POD特异性活性,并且几乎没有氧化酶(OXD)和催化酶(CAT)的模拟活性。因此,Fe3O4@COF@Os可以在生物基质中无背景干扰地分离和分析目标分子。研究还建立了基于Fe3O4@COF@Os的侧流免疫层析法(LFA)来检测血清中的癌症生物标志物前列腺特异性抗原(PSA),其检测限为3.83 pg mL^-1。在临床前列腺癌样本中,该方法的准确性达到100%,与商业ELISA试剂盒的相关系数为0.998。此外,该纳米酶还能检测低至0.1 µM的唾液葡萄糖,背景干扰可忽略且具有良好的可回收性。这种特定的磁性纳米酶为无需预处理的快速准确疾病诊断提供了一种有前景的POC策略。
研究背景:
1. 在生物传感领域,尤其是在疾病诊断中,传统的纳米酶模拟物(nanozymes)由于其复杂的样品基质和非特异性的多酶活性,容易产生背景信号干扰,降低了诊断的准确性。
2. 为了提高生物传感的特异性和准确性,学者们尝试了多种策略,包括单原子纳米酶、高熵纳米酶和纳米团簇酶等,以提高模拟过氧化物酶(POD)的催化效率和检测灵敏度。
3. 本研究开发了一种磁性和POD特异性的共价有机框架(COF)限域的锇(Os)纳米酶团簇Fe3O4@COF@Os,通过调节还原剂和COF配体的功能基团,实现了对Fe3O4@COF@Os催化活性和特异性的调控。该研究首次发现通过使用抗坏血酸作为还原剂和含氟功能COF配体,Fe3O4@COF@Os展现出卓越的POD特异性活性,并且几乎不具有氧化酶(OXD)和催化酶(CAT)模拟活性,从而在生物基质中实现无背景干扰的目标分离和分析。
实验部分:
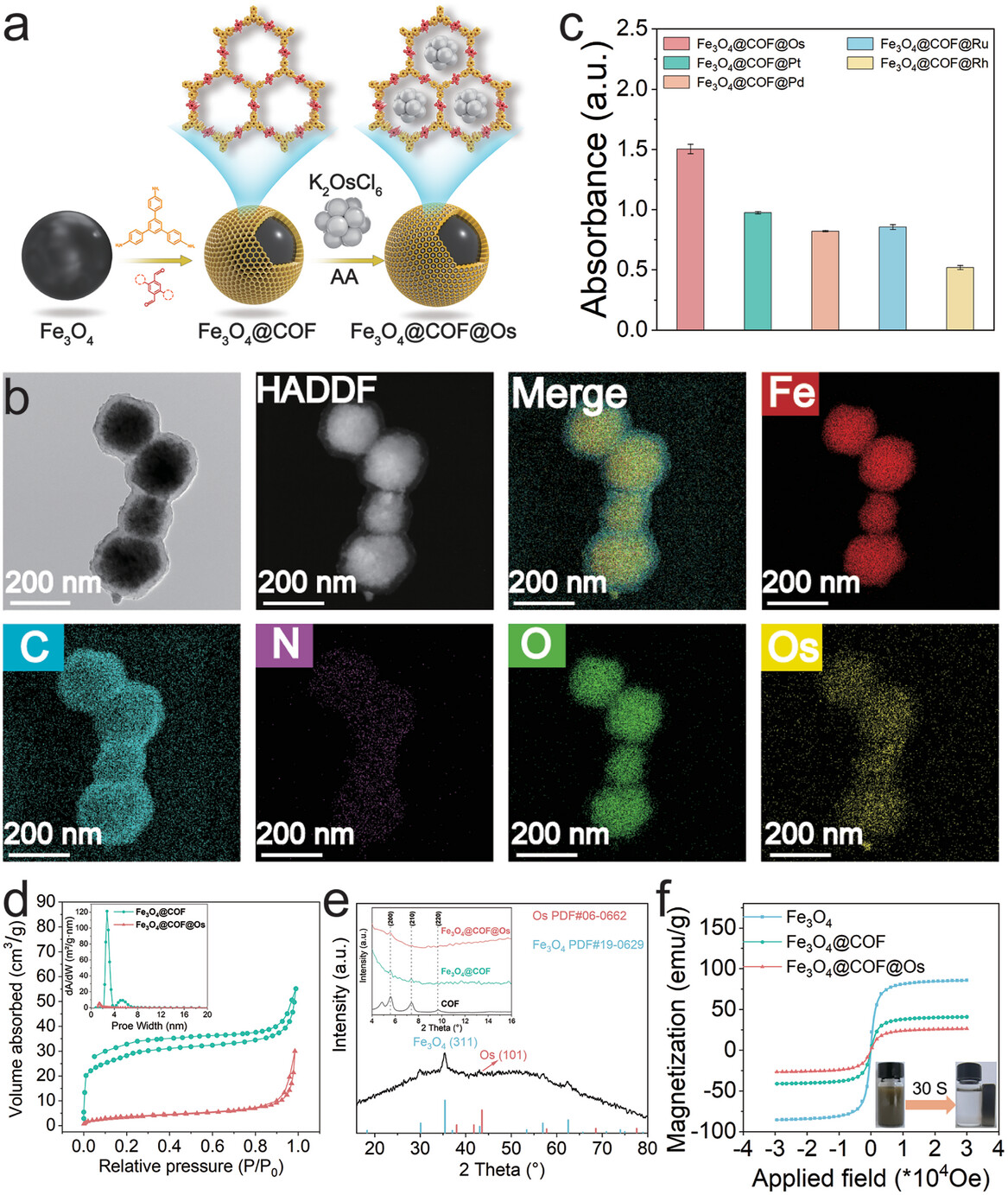
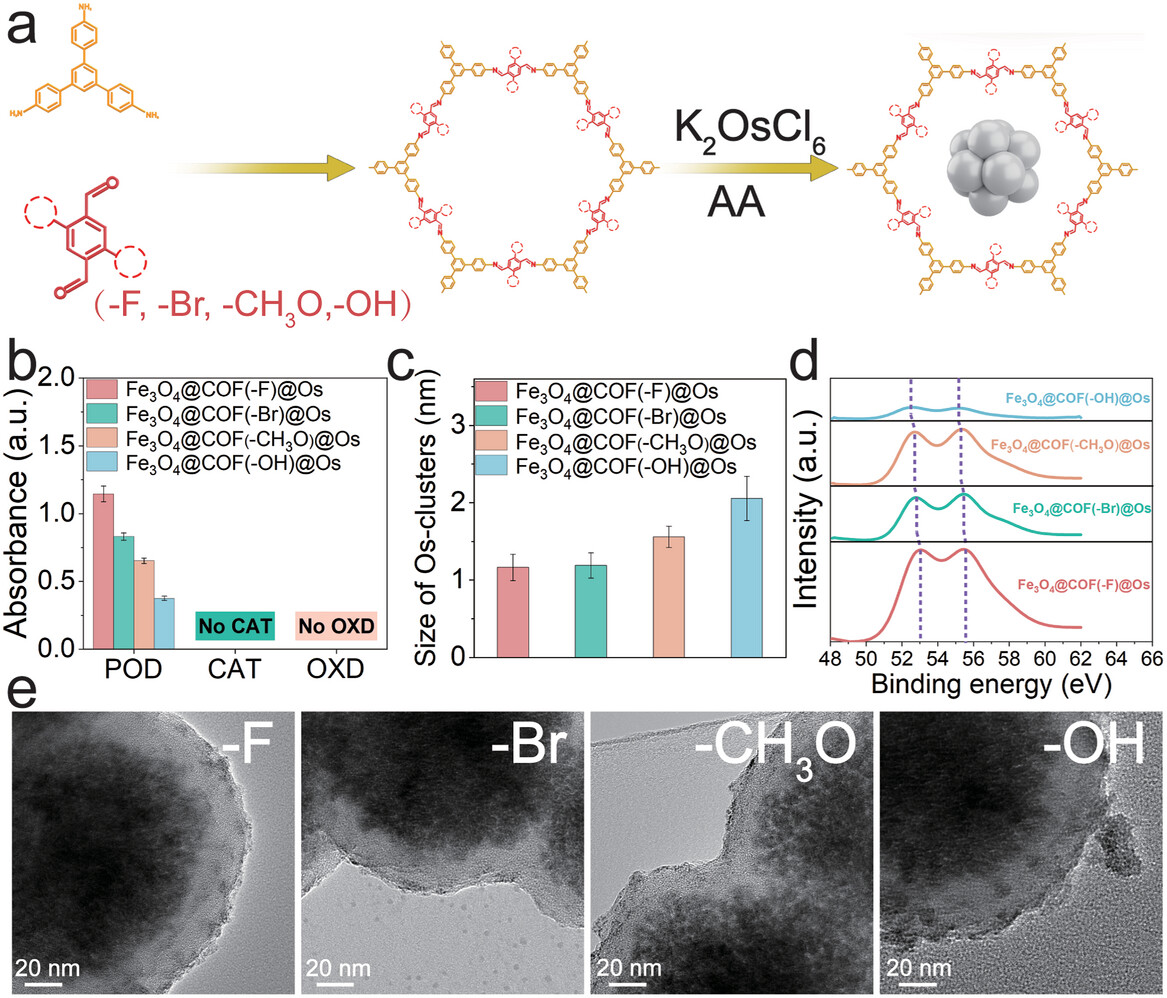
1. 合成Fe3O4@COF@Os纳米复合物:通过溶热反应方法合成Fe3O4纳米颗粒,随后在Fe3O4纳米颗粒上原位生长COF壳层,使用1,3,5-三(4-氨基苯基)苯(TAPB)和2,5-二氟对苯二甲醛作为配体。最后,通过抗坏血酸(AA)还原K2OsCl6在COF壳层中形成Os纳米团簇。
2. 表征纳米复合物:使用透射电子显微镜(TEM)和能量色散X射线光谱(EDS)对Fe3O4@COF@Os进行了形貌和元素分布的表征。通过动态光散射(DLS)测量了纳米复合物的ζ电位和水合粒子尺寸。通过紫外-可见光谱(UV-Vis)和X射线衍射(XRD)分析了纳米复合物的光学性质和晶体结构。通过振动样品磁强计(VSM)测试了纳米复合物的磁性能。
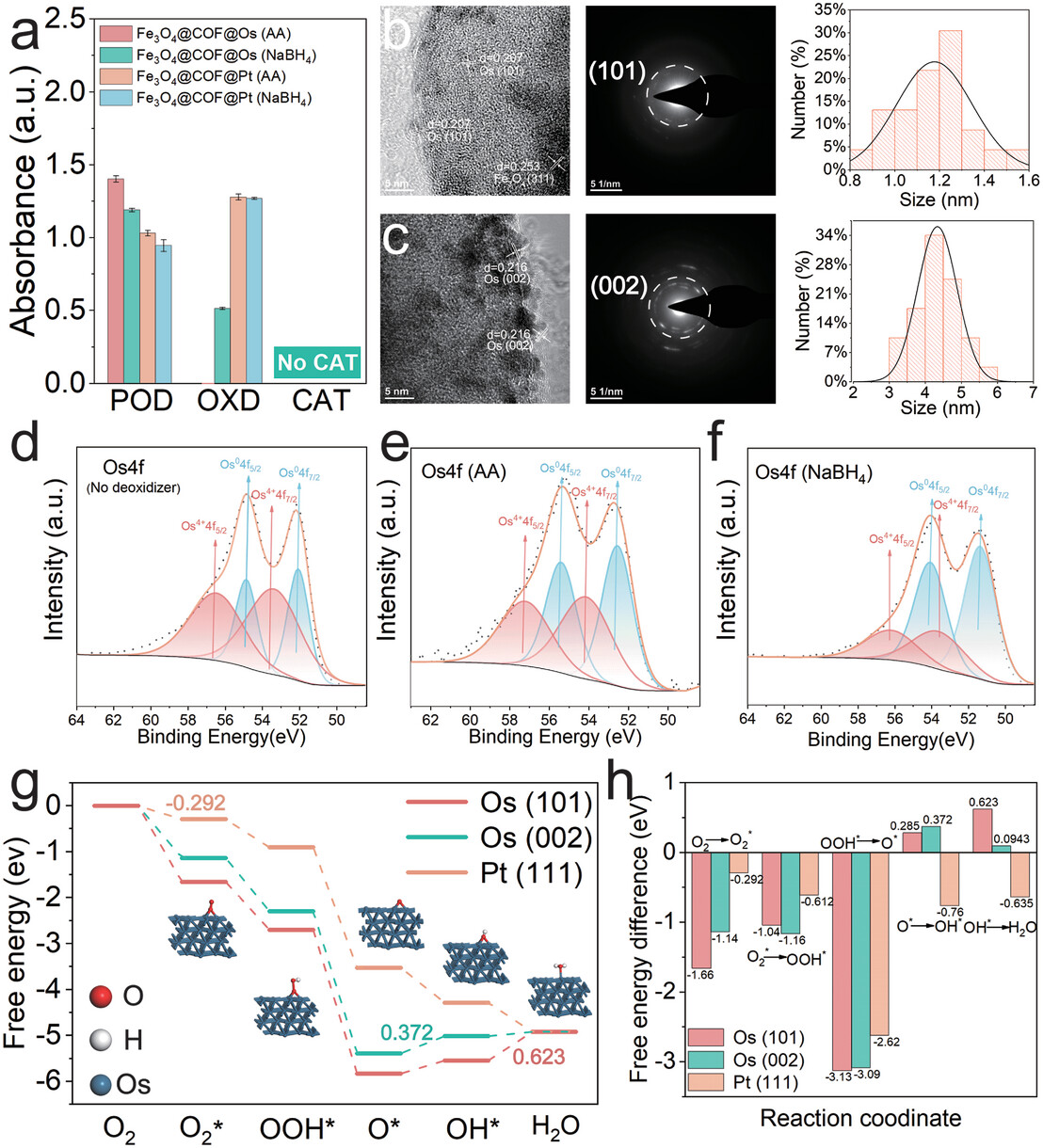
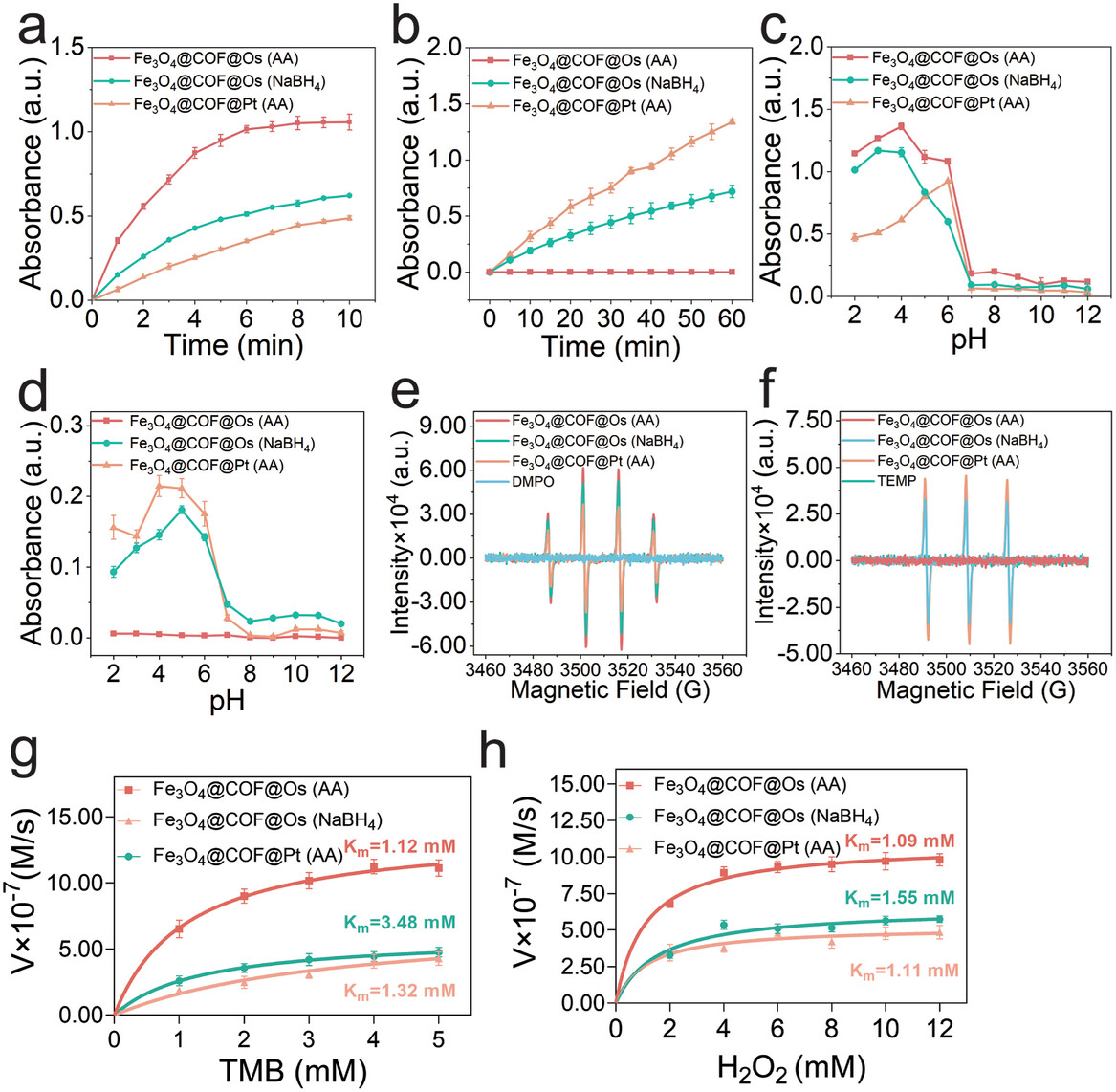
3. 催化活性和特异性调节:通过使用不同的还原剂(抗坏血酸和硼氢化钠)调控Fe3O4@COF@Os的POD模拟活性和特异性。通过密度泛函理论(DFT)计算探讨了不同还原剂对Os纳米团簇电子态和晶体结构的影响。
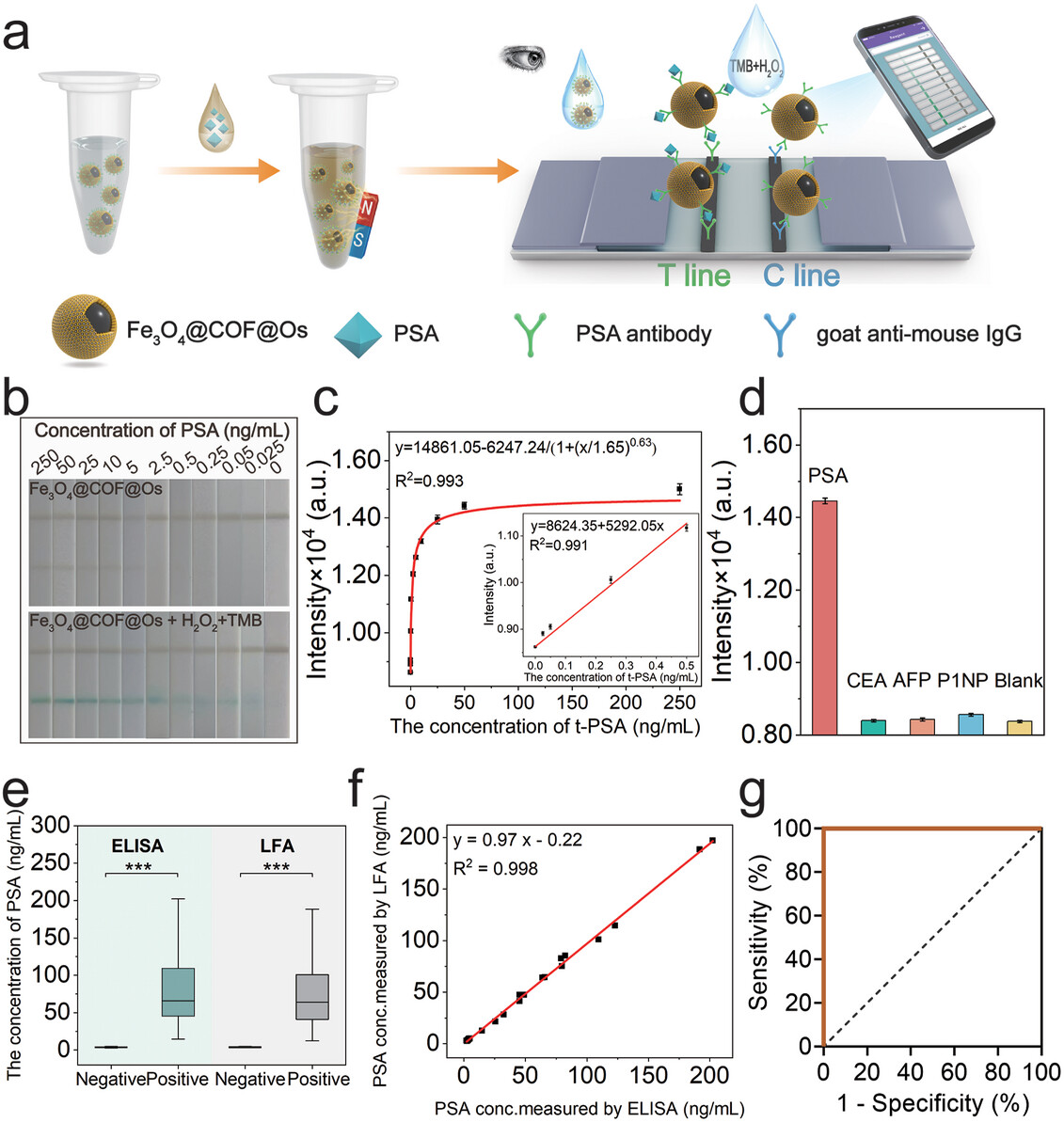
4. 生物传感应用:基于Fe3O4@COF@Os的高POD特异性活性,开发了用于检测血清中前列腺特异性抗原(PSA)和唾液中葡萄糖的侧流免疫层析法(LFA)。实现了对PSA的超灵敏检测,检测限为3.83 pg mL^-1,与商业ELISA试剂盒的检测结果高度一致。同时,能够在唾液样本中检测低至0.1 µM的葡萄糖,且具有良好的回收性。
分析测试:
1. 结构表征:通过TEM和EDS确认了Fe3O4@COF@Os纳米复合物的成功合成,COF壳层的孔隙结构为Os纳米团簇的限域提供了空间,同时Fe3O4@COF@Os表现出超顺磁性,有利于生物样品中目标分子的快速分离。
2. 催化活性和特异性:通过对比Fe3O4@COF@Os与其他常见金属纳米团簇(如Fe3O4@COF@Pt/Pd/Ru/Rh)的POD模拟活性,证实了Fe3O4@COF@Os具有最佳的POD模拟活性。通过改变还原剂,成功调节了Fe3O4@COF@Os的POD和OXD模拟活性,实现了在酸性检测环境中的POD特异性活性。
3. 生物传感性能:Fe3O4@COF@Os基于POD特异性活性,成功应用于PSA和葡萄糖的检测,展现了超高的灵敏度和特异性。通过LFA条带的可视化检测和智能手机软件的定量分析,实现了对疾病生物标志物的快速、准确检测。
总结:
本研究开发的Fe3O4@COF@Os纳米酶团簇作为一种新型的生物传感平台,具有显著的磁性分离能力、POD特异性活性和通过调节还原剂实现的酶特异性调控能力。该纳米酶团簇在复杂基质中对PSA和葡萄糖的检测表现出超高灵敏度和特异性,且具有快速、无需预处理和良好的回收性,为现场快速准确疾病诊断提供了有力的工具。
展望:
1. 进一步探索Fe3O4@COF@Os在其他生物标志物检测中的应用,以及在其他生物传感领域的潜在应用。
2. 对Fe3O4@COF@Os的长期稳定性和在更复杂生物样品中的性能进行深入研究,以确保其在实际应用中的可靠性。
3. 探索通过改变COF壳层的孔隙结构和功能基团,进一步优化Fe3O4@COF@Os的催化活性和特异性,以及探索其在生物医学领域的其他潜在应用。
Specific and Magnetic Covalent Organic Framework Confined Os Nanoclusterzyme for Interference-Free and Ultrasensitive Biosensing
文章作者:Pengyou Zhou, Yuwei Dai, Xiaorui Lin, Yuxin Song, Yuanfeng Pang, Rui Chen, Rui Xiao
DOI:10.1002/adfm.202400875
文章链接:https://onlinelibrary.wiley.com/doi/10.1002/adfm.202400875
本文为科研用户原创分享上传用于学术宣传交流,具体内容请查阅上述论文,如有错误、侵权请联系修改、删除。未经允许第三方不得复制转载。




